Ⅱ-2 乳癌領域
BRCA病的バリアントを有する乳癌患者に対し,乳房温存療法は条件付きで行わないことを推奨する。
エビデンスの確実性「中」/推奨のタイプ「当該介入に反対する条件付きの推奨」/合意率「73%(8/11)」
推奨文:本ガイドラインで実施したメタアナリシスの結果から,BRCA病的バリアントを有する乳癌患者における乳房温存療法は,散発性乳癌患者に比べて温存乳房内再発率が高いことが示された。この傾向は観察期間が長くなるほど明確になることから,温存乳房内の新規乳癌の発症リスクは長期にわたって継続するものと推察された。ただし生存率の悪化に関するデータは認めず,温存手術を強く希望し温存乳房の新規乳癌発症のリスクや継続的な温存乳房のスクリーニングの必要性等を理解したうえで選択する場合には,これを否定しない。
早期乳癌患者がBRCA病的バリアントを有する場合,乳癌の術式選択として将来の新たな発がんリスクも検討したうえで乳房全切除を選ぶか,すでに発がんしている乳癌に対する必要十分な治療として温存手術を選択するか,悩むことが多い。2020年4月に家族歴をもつ患者等にBRCA遺伝学的検査を行うことが保険適用となったことから,乳癌診断時にBRCA遺伝学的検査を受ける患者が増加傾向にある。整容性の観点からは乳房全切除後のインプラントを用いた乳房再建も保険適用となっており,またCRRM・インプラント再建も保険適用になったことから,以前とは臨床状況が大きく変わってきている。乳房温存療法を行うのか,患側の乳房全切除・再建を行うのか,両側の乳房全切除・再建を行うのか,限られた時間の中で,患者が納得のいく治療方針を選択していくことは容易ではなく,本CQは臨床上重要な検討課題であると考えられる。
BRCA病的バリアントを有する乳癌患者の治療方針を検討する際には,乳房全切除する場合を比較対象として,乳房温存療法を行うことがどれくらいのリスクがあることなのかを検討すること(B)が重要となる。その際,乳房温存療法は放射線治療を行うことが標準的であることから,放射線治療のリスクも検討したうえで術式選択を行う必要があり,温存療法を「温存乳房照射を伴う,乳房部分切除術」として検討・議論を行った。また,散発性乳癌患者が同様の乳房温存療法を受ける場合に比べて,BRCA病的バリアント保持者の場合どれくらいリスクが異なるのか(A)を知ることは,患者に情報共有を行いともに意思決定をしていくという観点において重要な視点であると考えられる。以上より本CQを検討する際,「BRCA病的バリアントに対する乳房温存療法を行う」という介入に対して,比較対象をA「散発性乳癌患者に対する乳房温存療法施行群」として差はないかという検討と,比較対象をB「BRCA病的バリアント保持者に対する乳房全切除群」として差はないかという2つの観点から各々アウトカムを設定し検討した。
本CQでは比較対象をA「散発性乳癌患者に対する乳房温存療法施行群」,B「BRCA病的バリアント保持者に対する乳房全切除群」とし,それぞれAについては「温存乳房内再発率」「対側乳癌発症率」「全生存率」「有害事象」「リスク低減」「費用対効果」「患者意向」を,B については「温存乳房内再発率」「全生存率」「費用対効果」「患者意向」を評価した。
A「散発性乳癌患者に対する乳房温存療法施行群」との比較では,「温存乳房内再発率」に関しては13編のコホート研究から定量的システマティックレビュー(メタアナリシス)を行って検討した。「対側乳癌発症率」に関しては12編のコホート研究,「全生存率」に関しては4編のコホート研究,「有害事象」に関しては1編のコホート研究,「リスク低減」に関しては1編のコホート研究を採用し定性的システマティックレビューを行った。B「BRCA病的バリアント保持者に対する乳房全切除群」との比較では,「温存乳房内再発率」に関しては3編のコホート研究,「全生存率」に関しては3編のコホート研究を採用し定性的システマティックレビューを行った。
まず,A「散発性乳癌患者に対する乳房温存療法施行群」との比較について示す。
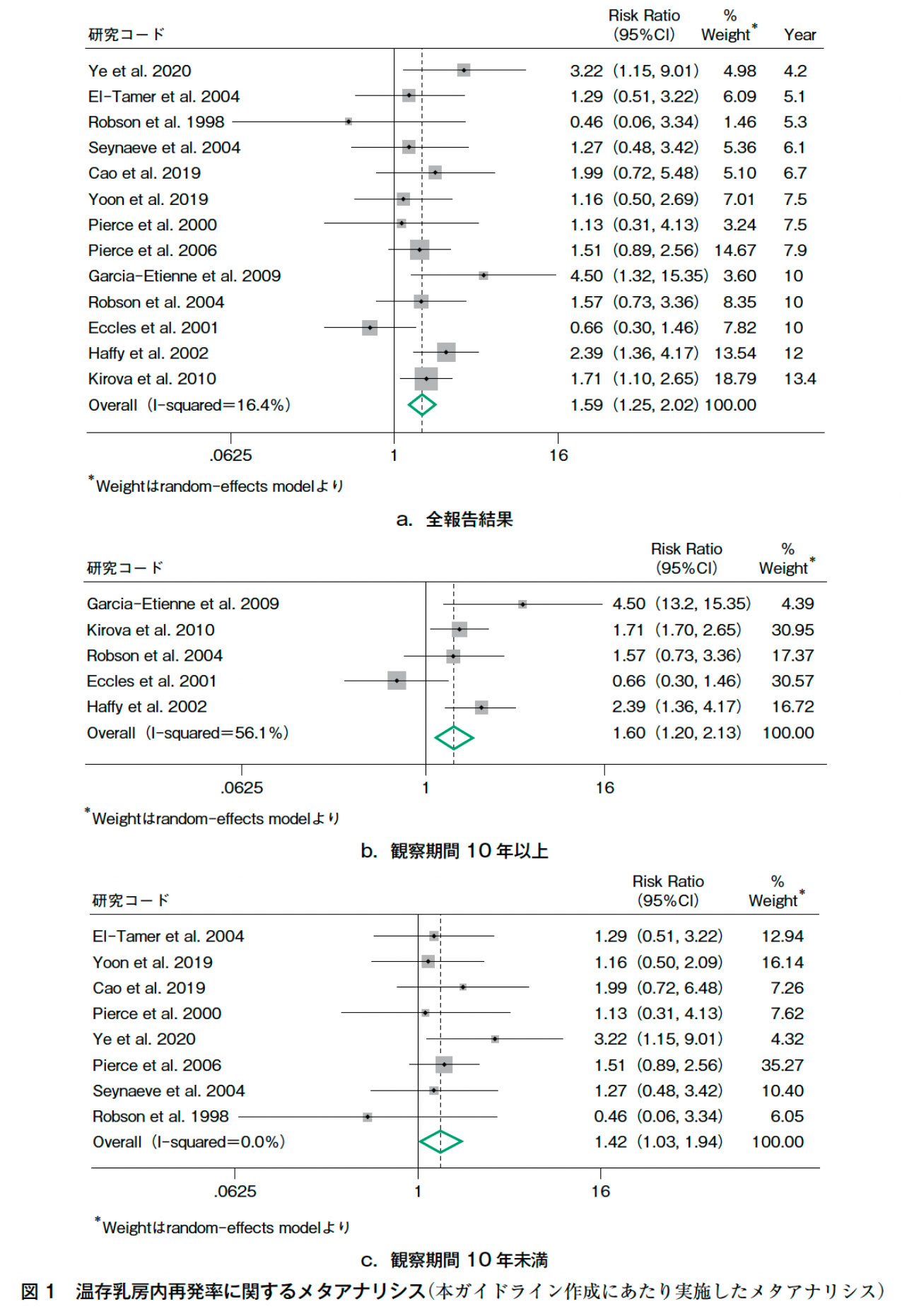
13編のコホート研究からメタアナリシスを行った(図1)1)~14)。今回のメタアナリシスでは,BRCA1/2病的バリアント保持者において,散発性乳癌患者と比較して乳房温存手術後の温存乳房内再発率は有意に高かった〔RR:1.589(95%CI:1.247—2.024)〕。また,観察期間別に行なった解析において,観察期間7年未満ではRR:1.491(0.932—2.385)と有意差は認めなかったが,7年以上の解析ではRR:1.505(1.184—1.913),10年以上の解析でもRR:1.601(1.201—2.132)と有意差を認め(図1b),10年未満のRR:1.42(1.03—1.94)(図1c)よりも高いRRとなっていた。統計学的異質性は低いこと,13編のコホート研究があったことから,エビデンスの確実性は強とした。
12編のコホート研究から定性的システマティックレビューを行った1)2)4)~6)8)~14)。散発性乳癌の温存療法に比べて,対側乳癌発症は有意に多いという報告が多かった。システマティックレビューおよびメタアナリシスが行われた文献では,対側乳癌についてはリスク比3.56(95%CI:2.50—5.08)とBRCA病的バリアントを有する群で有意に高いという結果であった。しかしアシュケナージ系ユダヤ人に限定した文献も散見され,観察群間でのステージ,年齢,卵巣摘出術の有無,術後療法等の調整がされていないものが多くバイアスの大きい結果であり,エビデンスの確実性は弱とした。
4編のコホート研究から定性的システマティックレビューを行った10)11)15)。BRCA1/2に分けて報告されていた論文はわずか1編のみであり,BRCA1病的バリアント保持群のHR:1.3(0.91—1.85),BRCA2病的バリアント保持群のHR:1.07(0.66—7.74)との報告であった。いずれにしてもアシュケナージ系ユダヤ人が含まれている文献も散見され,観察群間でのステージ,年齢,卵巣摘出術の有無,術後療法等の調整がされていないものが多くバイアスの大きい結果であった。以上よりエビデンスの確実性は弱とした。
1編のコホート研究から定性的システマティックレビューを行った6)。正常組織に対する安全性については急性期および晩期有害事象ともに差を認めなかった。1編の観察研究のみからの報告であることからエビデンスの確実性は弱とした。
1編のコホート研究から定性的システマティックレビューを行った9)。散発性乳癌の乳房温存療法と比べてタモキシフェン(TAM)内服より対側乳癌発症率は低下するとの報告であった。1編の観察研究のみからの報告であることからエビデンスの確実性は弱とした。
該当論文なし。
該当論文なし。
次に,B「BRCA病的バリアント保持者に対する乳房全切除群」との比較について示す。
3編のコホート研究から定性的システマティックレビューを行った16)~18)。乳房温存療法群では温存乳房内再発率が有意に高くなるとの報告を2編で認めた。しかし,「同側乳房内再発」や「局所再発」の定義を記載していない論文やイベント発生数が極端に少ない論文を含むこと,観察期間,観察群間でのステージ,年齢等の調整がされていないこと等からバイアスの大きい結果であり,エビデンスの確実性は弱とした。
3編のコホート研究から定性的システマティックレビューを行った16)~18)。観察期間,観察群間でのステージ,年齢等の調整がされていないものが多くバイアスの大きい結果であった。なお,BRCA1/2に分けて報告されていた論文はわずか1報のみであり,BRCA1のHR:1(0.56—1.76),BRCA2のHR:1.2(0.35—4.13)との報告であった。以上からエビデンスの確実性は弱とした。
該当論文なし。
該当論文なし。
本ガイドライン内で行ったメタアナリシスでは,BRCA1/2病的バリアント保持者において,散発性乳癌患者と比較して乳房温存手術後の温存乳房内再発は有意に高かった〔RR:1.589(95%CI:1.247—2.024)〕。また,7年以上の解析ではRR:1.505(1.184—1.913),10年以上の解析ではRR:1.601(1.201—2.132)と温存乳房内再発率は観察期間が長いほど有意に増加する傾向が認められたことから,若年のBRCA病的バリアントを有する乳癌患者に対する乳房温存療法には長期的な乳房内再発のリスクが高いことが示された。しかし温存乳房内再発は散発性乳癌患者の1.6倍であること,生存率に有意な差は認められないことからBRCA病的バリアントを有する患者に対する乳房温存療法を強く否定する根拠につながる結果は得られなかった。今回患者意向に関する文献の採用論文がなく,「乳房が温存されることに対する価値感」や「温存乳房への再発への恐怖・ストレス」等はエビデンスから検討することができず,今後の検討課題であると考えられた。
本CQの議論は,深刻な経済的・アカデミックCOIのない乳癌領域医師3名,婦人科領域医師2名,遺伝領域医師3名,遺伝看護専門看護師1名,認定遺伝カウンセラー1名,患者・市民2名の12名が参加した。投票は1名が棄権し,11名で行った。
BRCA遺伝学的検査の保険収載により,乳癌診断時に検査を受ける患者が増え,病的バリアントを保持することが乳癌診断と同時期に判明することが増えている。また乳房再建が保険外診療であった時代は,乳房温存療法が施行できない場合は乳房全切除術しか選択肢がなかったが,現在は乳房再建が保険適用となり,臨床状況はずいぶん変わってきている。投票では,「BRCA病的バリアントを有する乳癌患者において,術式選択の際に乳房温存療法を受けるリスクについて検討したうえで治療方針を検討することが臨床上重要である」ことを「はい」とするのが11 票であった。
望ましい効果については,「BRCA病的バリアントを有する乳癌患者が手術を受ける際,乳房が残ることに対してどの程度満足するか」という患者意向についての問いについて文献的考察はなかった。乳房温存療法を望んだときは「望ましい効果」として検討する必要があり,当事者の意見が重要であるという認識で一致した。議論に参加した乳癌体験者からは「乳房が残ることは患者にとっては望ましいことであり,乳輪を残すか,どこに傷が残るのかも重要である。残せるのであれば残したい。」という意見が出た。投票では意見が割れ,「分からない」6票,「さまざま」3票,「中」2票であった。
望ましくない効果については,本ガイドライン内で行われたメタアナリシスでも示された通り,長期フォローアップ中に温存乳房内再発が有意に多くなってくることがわかっており,散発性乳癌患者に対する乳房温存療法と同じ説明で選択することはできない。しかし全生存率に差がないという情報も大きな要素であるという意見が出た。以上から,A「散発性乳癌患者の乳房温存療法施行群」との比較で行われた検討に対する投票では,「大きい」7票,「中」3票,「分からない」1票であった。B「BRCA病的バリアント保持者に対する乳房全切除群」との比較で行われた投票では「中」10票,「分からない」1票であった。
温存乳房内再発率を重要なアウトカムと考えるとメタアナリシスの結果からエビデンスの確実性は「強」であったこと,他のアウトカムではエビデンスの確実性は「弱」であったことから,A「散発性乳癌患者に対する乳房温存療法施行群」との比較で行われた検討に対する投票では,「中」9票,「弱」2票であった。一方B「BRCA病的バリアント保有者に対する乳房全切除群」との比較では,採用文献が温存乳房内再発5編,全生存率3編ですべてコホート研究でありメタアナリシスできなかったことから,投票では「弱」6票,「非常に弱」5票であった。以上よりCQにおけるアウトカム全体に対するエビデンスの確実性は「中等度」と判断した。
患者の価値観に関する論文は抽出されなかった。術式選択には温存乳房内再発だけでなく患者のライフステージや人生観によって,乳房を残す,残さないに関する価値観は大きく異なることが想定され,残せる乳房を予防的に切除するということへの考え方も大きくばらつきがあると考えられる。また再発時の治療や薬物療法,仕事や日常生活への影響等も考えると大きくばらつきがあると考えられる。費用については放射線治療を伴う乳房温存療法における負担額(手術および放射線治療)は乳房全切除における費用負担(手術のみ)よりも高額である。以上から投票では「重要な不確実性またはばらつきあり」8票,「重要な不確実性またはばらつきの可能性あり」3票,未投票1名であった。
BRCA病的バリアントを有する乳癌患者が放射線治療を伴う乳房温存療法を行い,その後乳房内再発が起こり,乳房全切除術と併せて乳房再建術を行った場合,最初から乳房全切除術と併せて乳房再建術を行った場合に比べると,放射線治療後であることから整容性が下がることや,2度の手術になることを考えると,最初から乳房全切除術・乳房再建術を行うことがやや優位性があると判断されるという意見が出た。以上から投票では「比較対象がおそらく有意」9票,「さまざま」2票であった。
費用対効果についての検討論文は認められなかった。しかしBRCA病的バリアントを有する乳癌患者に対する乳房温存療法は温存乳房内再発をきたした場合は2度の手術になることから,費用対効果についての投票では「採用研究なし」8票,「比較対象がおそらく有意」2票であった。乳房の術式に関しては患者の意向が十分に尊重されるべきであるという意見が出た。しかしBRCA病的バリアントを有する乳癌患者に乳房温存療法を実施する際には,温存乳房内のサーベイランスとして造影MRI検査を年に一度行い,早期の段階で診断する必要があることから,術式として単純に施行可能かどうかや,遺伝カウンセリング体制が整っているだけではなく,その後のフォローを適切に行うことができる施設で行うべきであり,全国どこでも体制が整っている状況ではないことも考慮すべきであるという意見が出た。以上から,容認性についての投票では「はい」7票,「おそらく,はい」2票,「おそらく,いいえ」1票,「さまざま」1票,実行可能性についての投票では「おそらく,はい」8票,「はい」2票,「分からない」1票であった。
以上より,BRCA病的バリアントを有する乳癌患者において,乳房温存療法は推奨されるかについて議論し,推奨草案は以下とした。
8/11名(73%)で推奨草案を支持し,採用が決定した。なお,投票では「当該介入もしくは比較対象のいずれかの推奨」を3名が支持した。
推奨決定会議では「当該介入に反対する条件付きの推奨」を支持する理由として,温存乳房内再発率が高くなるということを十分説明したうえでの意思決定が必要であること,結果の一貫性があり,長期生存期間中のフォローアップでリスクが高まることは明らかであること,生存率の差は認められなかったが,データが未成熟ということを反映している可能性があること,温存乳房内再発が早期に発見できることが重要であるが,早期に発見できるのかという問題があること,早期でも薬物療法が必要なこともあり,乳房温存をする場合は十分な説明のうえでの希望であるか,という観点が必要であると考えられた。最終的なアウトカムが最も重要ということではなく,主治医が十分説明して患者と協働意思決定していくというプロセスが最も重要になってくる。このような議論が多方面で行われることが重要であり,乳房温存を選択した患者がその後全摘することになったとしても,乳房が温存されていた時間がその人にとってよかったと感じる方もいるし,一度の手術で終わったほうがよかったと悔やむ方もいる。今回得られたエビデンスや議論をもとに,今後新たなクリニカルクエスチョンを作り,エビデンスを作っていくことが重要なのではないかという意見が出た。
一方,「当該介入もしくは比較対象のいずれかの推奨」を支持する理由として,生存率のデータが確約できていない以上,患者の気持ちが反映されるのであれば乳房を残す道も残してほしいという意見があり,意思決定のプロセスが重要である。また,再発リスクが高くなることがよくわかったが,2割は温存乳房内再発が起こり,8割は再発しないという捉え方もあるという意見が出た。
ASCOガイドライン2020では,BRCA病的バリアント保持者であることで部分切除を適応外とすべきではないという提言がなされている。明らかに乳房内再発は散発性乳癌に比べて多いがそのほとんどが再発ではなく,新規の病変であり,乳房温存療法は安全に施行されると結論付けられている。また全生存期間でのリスクについては長期的観察が必要であるとされている。ESMOガイドライン2010では,予防卵巣切除を行ったBRCA病的バリアント保持者が部分切除と放射線照射を受けた場合,乳房内再発リスクは散発性乳癌と同程度であるという報告から許容範囲であるとされている。
BRCA病的バリアント保持者にとって本介入により全生存期間の差があるかについて,引き続きモニタリングが必要である。またBRCA1,BRCA2に分けて検討されるべきである。
関連学会より,推奨文中の表現に関するご指摘を受け,当該部位を修正した。
BRCA,breast neoplasms,mastectomy,breast conserving surgery,cost,patient preference,patient satisfaction,complication
