Ⅱ-3 卵巣癌領域
BRCA1/2 病的バリアント保持者に対し, RRSO を実施することを条件付きで推奨する。
推奨のタイプ:当該介入の条件付きの推奨
エビデンスの確実性:強,合意率:91%(11/12 名)
推奨の解説: BRCA1/2 遺伝子病的バリアントを保持する女性は乳癌や卵巣癌の発症リスクが高い。 BRCA1/2 遺伝子病的バリアント保持者にとって RRSO は,有効なサーベイランス方法が確立されていない卵巣癌のがん死低減効果が認められること,また乳癌発症予防効果が確認されていることより重要な選択肢といえる。一方, RRSO により起こる妊孕性の喪失や様々な女性ヘルスケアの問題についてはいまだエビデンスが十分とはいえない状況にある。
BRCA1/2 遺伝子病的バリアントを保持する女性は乳癌や卵巣癌等の発症リスクが高く,とりわけ卵巣癌に関しては早期発見のための有効なサーベイランス方法は確立されていない状況にある。 BRCA1/2 遺伝子病的バリアント保持者に対する卵巣癌発症予防のための方法として,正常な卵巣,卵管を外科的に切除する RRSO が検討されている。また, RRSO は乳癌発症の予防や,乳癌特異的死亡率に影響することがわかってきた。
一方で,正常な臓器を摘出すること,また摘出することで起こる妊孕性の喪失や卵巣欠落症状等の合併症への不安,女性としてのアイデンティティ,女性ヘルスケアの問題等,様々な不利益に対しても配慮する必要がある。
以上より,この問題に取り組むことは優先度が高いと考える。
「卵巣癌発症リスクの低減効果」「全生存期間(OS)」「乳癌発症リスクの低減効果」「乳癌特異的死亡率の低下」「合併症」「費用対効果」「患者の意向」「患者の満足度」を評価した。
「卵巣癌発症リスクの低減効果」「全生存期間(OS)」については 2 編のメタ解析, 3 編の前向きコホート研究を採用した。「乳癌発症リスクの低減効果」「乳癌特異的死亡率の低下」について 2 編のメタ解析を採用した。「合併症」については 4 編のコホート研究,「費用対効果」についてはメタ解析 1 編を含む 2 編の論文を採用した。「患者の意向」「患者の満足度」については 4 編の論文を採用した。
卵巣癌発症予防に関する RRSO のエビデンスとして採用した 2018 年のメタ解析では, 3 編の前向きコホート研究(観察期間 0.5~27 年)に参加した 2,534 人の BRCA1/2 病的バリアント保持者において, RRSO 実施者は非実施者と比較し,卵巣癌発症のリスク低減効果が確認された〔ハザード比(hazard ratio:HR):0.06(95%CI:0.02-0.17,P<0.001)〕1)。
【エビデンスの確実性:強】
また, RRSO 実施者は非実施者と比較し,全生存期間(overall survival:OS)の延長が確認された〔HR:0.32(95%CI:0.19-0.54,P<0.001)〕1)。 2019 年のメタ解析では,乳癌未発症と既発症に分けて検討したが,いずれにおいても OS の延長が確認された〔HR:0.27(95%CI:0.10-0.43),HR:0.33(95%CI:0.28-0.38)〕2)。
【エビデンスの確実性:強】
2023 年の Gaba らのメタ解析3)では, BRCA1/2 病的バリアント保持者全体において原発乳癌リスク〔RR:0.84(95%CI:0.59-1.21)〕,対側乳癌リスク〔RR:0.95(95%CI:0.65-1.39)〕いずれもリスク低減はみられない。サブグループ解析では BRCA1 のみの原発乳癌リスク低減効果はみられないが, BRCA2 のみにおいてはリスク低減効果がみられる〔RR:0.63(95%CI:0.41-0.97)〕。対側乳癌リスクはいずれもリスク低減効果はみられない。また,閉経前後で検討も行っているが,いずれもリスク低減効果はみられていない。
Wang らが 2022 年に報告したメタ解析4)では, BRCA1 , BRCA2 病的バリアントともに乳癌リスク低減効果を認めた〔 BRCA1 のみはHR:0.63(95%CI:0.49-0.81,P<0.01), BRCA2 のみはHR:0.51(95%CI:0.34-0.75,P<0.01)〕。これらの結果は一貫性が高いにもかかわらず,感度分析は個々の研究を 1 つずつ除外した後でも結果を確認できた。サブグループ解析において RRSO のタイミングについて検討している。 50 歳をカットオフ値として, 50 歳未満での RRSO , 50 歳以上での RRSO を検討し, 50 歳未満では BRCA1 BRCA2 ともに RRSO による乳癌発症リスク低減効果を認める〔 BRCA1 はHR:0.48(95%CI:0.30-0.77,P<0.01), BRCA2 はHR:0.22(95%CI:0.08-0.65,P<0.01)〕が, 50 歳以上で BRCA1 , BRCA2 ともにリスク低減効果は認めなかった。 RRSO からの期間については,カットオフ値を 5 年とし, RRSO 術後 5 年未満では BRCA1 , BRCA2 ともに RRSO による乳癌リスク低減を認め〔 BRCA1 , BRCA2 BRCA1 はHR:0.60(95%CI:0.40-0.89,P=0.01), BRCA2 はHR:0.42(95%CI:0.20-0.86,P=0.02)〕, RRSO 術後 5 年以上では BRCA1 , BRCA2 いずれも RRSO 未施行群と RRSO 群の間に明らかな乳癌発症の差は認めなかった。これらのメタ解析以外にも, RRSO による乳癌発症リスクの低減効果については検討されてきたが,結論が一致していない。これについて, Gaba らは,研究対象の性質上,ランダム化比較試験は不可能であるため観察研究による GRADE の制限,過去のメタ解析内の重複するデータセット,様々な選択バイアスの存在等が原因である可能性を示唆している3)。
【エビデンスの確実性:中】
Gaba らの報告3)では, BRCA1/2 病的バリアント保持者全体における RRSO による乳癌発症リスクの低減効果は認められなかったが,乳癌特異的死亡率は低下する〔RR:0.26(95%CI:0.18-0.39)〕。また,サブグループ解析において BRCA1 病的バリアント保持者における乳癌特異的死亡率についてもリスク低減効果を認めた〔RR:0.46(95%CI:0.30-0.70)〕。
【エビデンスの確実性:強】
RRSO による合併症を,①骨折,骨粗鬆症,②更年期症状,③心血管リスク,④ RRSO 後 HRT による乳癌発症リスクについて,それぞれコホート研究が 1 編ずつ報告されている。
【エビデンスの確実性:中】
(1)骨折・骨粗鬆症
中央追跡期間 6.9 年以内では BRCA1/2 病的バリアント RRSO 群での骨折リスク増加なし(HR:0.80)骨粗鬆症の診断リスクは高い(HR:1.83)5)。
(2)更年期症状
RRSO 実施 3 カ月後のホットフラッシュの有病率は 5.3%から 56.2%に増加し,夜間の多汗症は 20.2%から 47.2%に増加。症状は 3 カ月から 12 カ月の間に悪化せず, RRSO 未施行群比較群では変化なし(P<0.001)。 RRSO の後,ホルモン補充療法(hormon replacement therapy:HRT)使用者は非使用者よりも QOL が向上した〔調整済み係数:0.49(95%CI:0.20-0.78)〕6)。
(3)心血管リスク
BRCA1/2 病的バリアント保持者と良性疾患で卵巣摘出を受けた女性の間で心血管疾患のリスクは有意差なし7)。
(4)RRSO 後HRT による乳癌発症リスク
Marchetti らのメタ解析では,乳癌未発症の RRSO 後女性への HRT による乳癌発症リスクの上昇は示されていないが8), 45 歳以上ではリスクが上昇したというコホート研究がある9)。詳細は卵巣癌 CQ6 を参照。
費用対効果について,検討しているのは 2 論文であった。 RRSO 単独でも費用対効果があると結論されている。 BRCA1 では 35 歳での RRSO が 2,101 ドル/質調整生存率年(quality adjusted life year:QALY), BRCA2 では 40 歳での RRSO が 5,535 ドル/QALY と,それぞれ費用対効果が高かった。これには,乳癌発症関連のみではなく卵巣癌発症関連の費用も含まれている10)。コホート研究1 論文では, RRSO を含む予防措置は,サーベイランス強化群と比べて, QALY および生存年(LY)の増加によりコスト削減につながると結論されている。ただし,スイスにおける費用の算出結果であり,保険制度の異なる日本においては,直接性が劣ると判断した11)。
費用対効果とは異なるが,実施率に関しては,保険適用前後の RRSO 実施率の変化について検討しているものが 2 論文あった。保険適用後のほうが HBOC における RRSO 施行率が上昇〔保険適用前:29.1%,保険適用後:61.1%(P=0.039)〕した。保険適用により RRSO 施行率が上昇という報告は,いずれも国内のコホート研究であり,保険適用になってからの RRSO 実施率は上昇したと結論付けられている12)13)。
【エビデンスの確実性:中】
日本のみのデータでは, HBOC の約 30%が RRSO を受けている14)。RRSO を選択するかの過程は複雑である。 BRCA1/2 病的バリアント保持者や閉経後,乳癌既往のほうが RRSO を選択する傾向があった15)。 BRCA 遺伝学的検査を受ける時の年齢16),決断するときの年齢, BRCA1/2 の病的バリアント, RRSO に対する情報の捉え方(リスク低減等), RRSO を施行せずスクリーニングを行うことの限界,卵巣癌の罹患の不安,手術合併症,更年期症状の不安,不妊,女性としてのアイデンティティ等が関係している17)。
【エビデンスの確実性:弱】
BRCA1/2 病的バリアント保持者で RRSO 後,経時的に満足度を調べると,最終的(RRSO 後,平均1.8 年)な満足度は高いという報告はあるが,単施設のデータで症例数が少なく,最終までフォローできている症例率が低い18)。
RRSO の効果として評価されるべき OS の延長は確認されているが,今後長期的なヘルスケアの満足度評価が必要である。
【エビデンスの確実性:弱】
メタ解析の結果から, BRCA1/2 病的バリアント保持者に対する RRSO は,卵巣癌卵管癌の発症予防リスク低減効果と OS の延長効果を認めることは確実と判断した。
乳癌発症リスクについて,システマティックレビュー 2 本においてアウトカムの設定が異なるため結果が一致していないが,少なくとも 45 歳以下では RRSO による新規乳癌発症リスクは低下すると考えられる。また,乳癌特異的死亡率についても RRSO による低減効果は認めると考えられる。
費用対効果については国内からの報告がなく,直接的な経済効果について明確でない。しかしながら,保険適用後の実施率は実際に向上していることがわかった。
RRSO による合併症について,骨粗鬆症のリスク,ホットフラッシュの有病率は上昇するものの,骨折のリスク増加はなく,また更年期症状は HRT による改善も認められている。心血管リスクも RRSO によるリスク増加はみられない。 RRSO 後 HRT での乳癌発症リスクは 45 歳以下においては乳癌発生率に影響はないが, 45 歳以上においては, HRT 使用者の乳癌発生率が非使用者よりも高い可能性がある。
本 CQ の推奨決定会議参加対象委員 12 名の内訳は,乳癌領域医師 2 名,婦人科領域医師 2 名,遺伝領域医師 2 名,遺伝看護専門看護師 1 名,認定遺伝カウンセラー 2 名,患者・市民 3 名であった。推奨決定会議の運営にあたっては,事前に資料を供覧し,参加対象委員全員が Evidence to Decision フレームワークを記入して意見を提示したうえで,当日の議論を行った。推奨決定会議には参加対象委員全員が参加した。
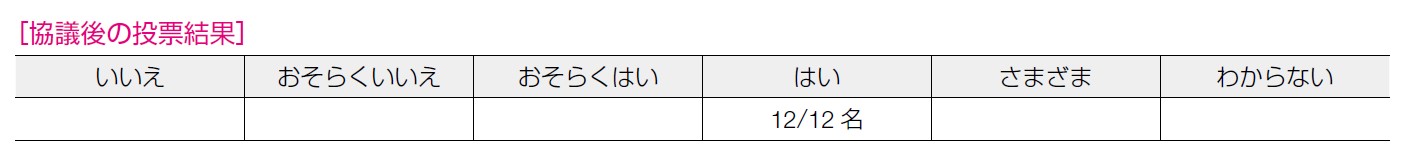
本 CQ が優先事項かについては 12 名全員が「はい」と回答した。卵巣癌に関して早期発見のための有効なサーベイランス方法が確立していない状況で,心理的な負担も当事者にとって大きいと考えられる。また,卵巣癌のがん死低減効果のみでなく,副次目的の乳癌発症リスクも検証すべきであることが確認された。
12 名全員が「介入の望ましい効果」は「大きい」と回答した。卵巣癌の発症予防リスク低減効果,がん死低減効果を認めることは確実であり,乳癌発症予防効果が確認されていることも重要と判断された。施行年齢について本邦での推奨年齢を設ける必要があるのではないか,という意見もあった。

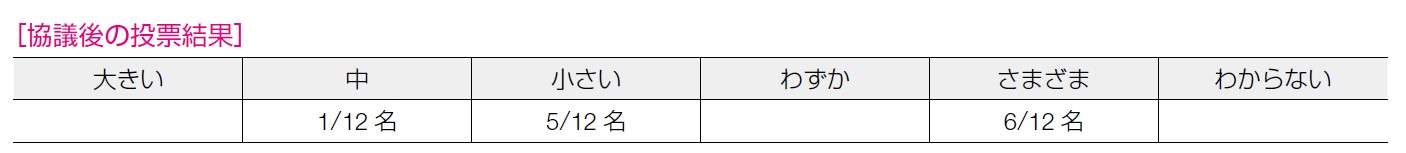
6 名が「さまざま」, 5 名が「小さい」, 1 名が「中」と回答した。がん死低減効果の大きさに比べて相対的に「小さい」という考え方や, QOL 低下に関する報告は乏しいという意見があげられた。一方で,卵巣欠落症状への不安・不妊・女性としてのアイデンティティ等の受け止め方は多様であること,更年期症状に対しては乳癌患者では HRT が行いにくいことから,「さまざま」であるという意見があげられた。「挙児希望がない」ことが前提となるが,乳癌発症後の化学療法・ホルモン治療のために月経が再開しない人も多く,また,卵子提供で 50 歳以上の分娩も増えており,挙児希望がなくなるタイミングを決めること自体が難しくなっている点も議論された。
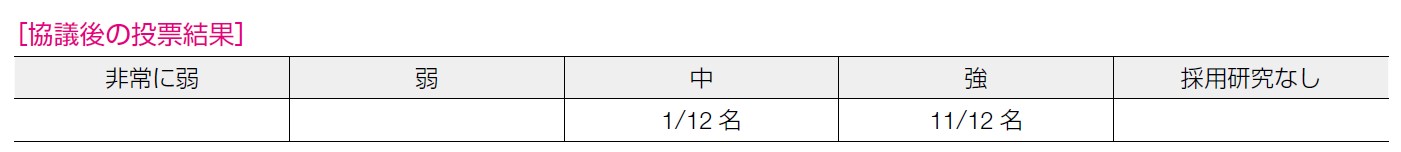
11 名が「強」, 1 名が「中」と回答した。卵巣癌リスクに対するエビデンスは強いが,乳癌発症リスクについてはアウトカムに完全の一致はみておらず,エビデンスレベルは下がるという意見が多かった。その中で,本来の卵巣癌によるがん死低減効果としてのエビデンスが主たるアウトカムであり,乳癌のエビデンスをもとにエビデンスの確実性を下げないほうが適切であると考えられた。
12 名全員が,「重要な不確実性またはばらつきの可能性あり」と回答した。患者の意向や満足度に関するエビデンスは不足しており,年齢や背景,ライフスタイルによって価値観は異なってくると考えられる。乳癌の後治療も個々に異なっており, RRSO 後の卵巣欠落症状が強く出る場合と出ない場合があることも不確実性につながる,という意見があげられた。

7 名が「介入が優位」, 5 名が「おそらく介入が優位」と回答した。医学的にリスク低減効果が示されている点で介入が優位と考えられる一方で,合併症等が生じることや推奨年齢についての記載がない中では「おそらく」という表現が必要という意見があげられた。

12 名全員が「介入が優位」と回答した。費用対効果に関してわが国からも報告が出ている。

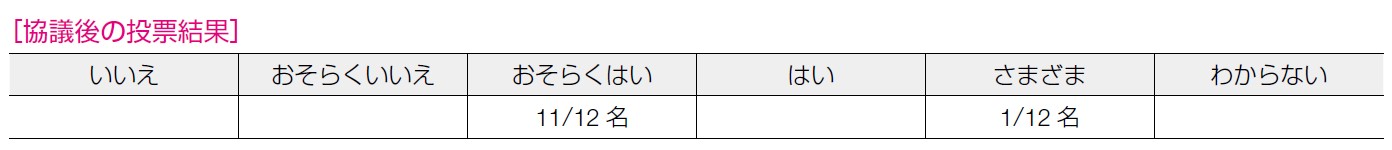
11 名が「おそらくはい」, 1 名が「さまざま」と回答した。意思決定においては様々な条件,プロセスがあり,個人の価値観,背景,年齢も影響する。卵巣欠落症状への拒否感,女性としてのアイデンティティ等, RRSO に対して容認できないと考える立場の人がいることを踏まえて判断するべきという意見が出された。
8 名が「おそらくはい」, 4 名が「はい」と回答した。日本婦人科腫瘍学会より,実施施設の体制についての考え方が示されており,施行可能な施設は増えているが,体制は施設によりさまざまである,という意見も出された。
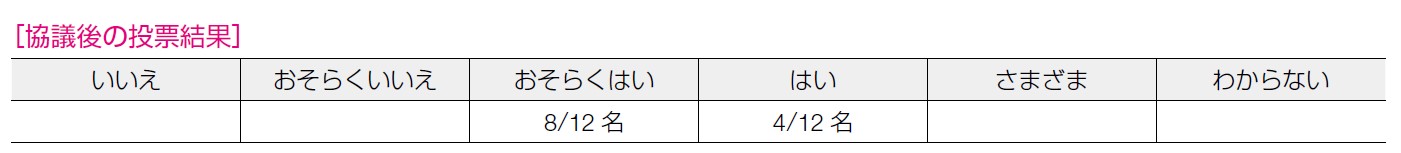
本 CQ の推奨タイプは「当該介入の条件付きの推奨」が11 名,「当該介入の強い推奨」が1 名であった。
「条件付き」とした理由として,女性ヘルスケアのエビデンスが少ない点,遺伝診療体制,適切な手術体制のもとで実施すべきである点があげられた。さらに,受精卵を凍結する選択肢についても議論がなされた。
なお実地臨床では,卵巣機能を失った後に妊娠する人が増加しつつあり,高年齢の妊娠管理が重要なテーマとなっている。 2023 年に発表された NCCN ガイドライン19)には「after child bearing」という文言は記載されておらず,「挙児希望がない」という用語の定義については慎重な判断が求められる。関連学会との意見交換も重要である,という意見が出された。

わが国の卵巣がん・卵管癌・腹膜癌治療ガイドライン20)では,乳癌未発症の BRCA1 あるいは BRCA2 病的バリアント保持者に対して, RRSO は遺伝カウンセリング体制ならびに病理医の協力体制が整っている施設において倫理委員会の審査を受けたうえで,婦人科腫瘍専門医が臨床遺伝専門医と連携して行うことを推奨している。
乳癌診療ガイドライン21)では, RRSO による乳癌発症リスク低減効果については不確実であるが,卵巣癌,卵管癌の発症予防効果, OS の延長効果を認めるため強く推奨するとされている。
NCCN ガイドライン19)では, BRCA1 の病的バリアント保持者は 35~40 歳の間, BRCA2 の病的あるいは病的である可能性が高いバリアントを保持する患者の卵巣癌の発症は, BRCA1 の病的あるいは病的である可能性が高いバリアントを保持する患者に比べて平均 8~10 年遅いため, BRCA2 の病的あるいは病的である可能性が高いバリアントを保持する患者では,家族内での卵巣癌診断年齢が予防手術を検討する年齢より早期ではない限り,卵巣癌リスク管理のための RRSO を 40~45 歳まで遅らせるのが妥当とされている。
ESMO * ガイドライン22)においても, RRSO は, BRCA1 病的バリアント保持者では 35~40 歳で実施, BRCA2 病的バリアント保持者では 40~45 歳で実施すべきとされている。
ESMO:European Society for Medical Oncology
RRSO を実施する際の心理的社会的影響については,当事者の病態,家族背景,年齢等の背景因子が複雑で現在のところ大規模な比較検討は実施されていない。現状では,当事者の状況や多様な価値観を配慮して診療をしていく必要がある。
RRSO 実施後に起こる女性ヘルスケアについてのエビデンスはまだ十分とはいえず,今後の研究課題である。また,妊孕性の問題については,今後がん生殖分野と連携し,受精卵凍結・将来的な妊娠等に関しての検討も課題である。
現在本邦では,乳癌既往の BRCA1/2 病的バリアント保持者に対して保険診療で RRSO を実施することができる。検討された研究ではがん既発症者,未発症者ともに RRSO 実施の効果が確認されているが,現時点で本邦では未発症者に対する RRSO は自費で行われている。また,乳癌再発患者についての検討はできていない。
外部評価団体より指摘を受け,当該箇所を修正した。
乳癌:BRCA,breast neoplasms,risk reducing bilateral salpingo-oophorectomy,breast cancer specific survival,complication,cost,patient preference,patient satisfaction
卵巣癌:BRCA,genetic counselling,RRSO,pathogenesis,cost,patient preference
文献検索式,エビデンス総体評価シート,システマティックレビューレポート,Evidence to Decisionフレームワークは,JOHBOC ホームページに掲載。
