Ⅱ-5 膵癌領域
BRCA1/2 病的バリアントを保持するプラチナ製剤感受性切除不能膵癌に対し,PARP 阻害薬の維持療法は条件付きで推奨する。
推奨のタイプ:当該介入の条件付きの推奨
エビデンスの確実性:中,合意率:100%(10/10 名)
推奨の解説:本CQ の推奨決定会議では,最も重要で影響の大きいPOLO 試験の結果を中心に議論を行った。同試験では,統計学的に有意な全生存期間(OS)の延長効果は示されなかった点,日本人が参加していない点,プラセボ対照の研究デザインである(日常診療ではプラチナレジメンが一定の効果を示したのち,無治療経過観察が選択されることは少ない)等,得られたエビデンスの解釈は慎重にすべきとの意見があった。また,膵癌に関わるすべての臨床医ががん診療の一部として遺伝性診療の実践が行えることを拡充していくことが大切である。
以上の議論から,本CQ に対する推奨は条件付きが妥当と判断され,POLO 試験で得られたエビデンスの適切な解釈と遺伝外来紹介を含む遺伝性腫瘍の患者・家族への適切な対応がその条件として推奨された。
医療技術の進歩にもかかわらず,膵癌は依然として予後不良な疾患である。以前より一部家系内に膵癌が多発する事例が報告されてきた。近年になり複数の生殖細胞系列病的バリアントと膵癌の関連も報告され,遺伝的要因が原因で膵癌を発症する患者が数%含まれることがわかってきた。生殖細胞系列病的バリアントとして最も頻度が高いのがBRCA1/2 で3~6%にみられることが知られている1)2)。そのため,膵癌もHBOC 関連がんに含められている。他のHBOC 関連がん同様,プラチナ製剤やPARP 阻害薬の有効性が示されている。
生殖細胞系列BRCA1/2 病的バリアントを保持する膵癌患者のプラチナレジメンの有効性については前向きのランダム化試験の結果はないが,プラチナレジメンの投与歴は治療ラインにかかわらず生存期間の延長と正の相関があるというメタ解析を含む複数の報告がある3)4)。PARP 阻害薬については前向き第Ⅲ相ランダム化試験(POLO 試験)が一遍報告されている5)。同試験では,生殖細胞系列BRCA1/2 病的バリアントの保持者で,一次治療のプラチナレジメンで16 週以上病状進行が抑えられた遠隔転移を有する膵癌患者に対し,オラパリブ維持療法とプラセボ群との治療成績を比較した。その結果,オラパリブはプライマリーエンドポイントである無増悪生存期間を延長することが示された〔中央値:7.4 カ月vs. 3.8 カ月,HR:0.53(95%CI:0.30-0.83)〕。生活の質(quality of life:QOL)スコアに関してもプラセボ群と有意差はなかったと報告されている。全生存期間(overall survival:OS)では統計学的な有意差を認めなかったが,これに関しては後治療の関与も推測される。後治療を受けた患者の割合はオラパリブ群では48.9%であったのに対しプラセボ群は74.2%と多く,さらにプラセボ群では14.5%の患者がPOLO 試験外でPARP 阻害薬の投与を受けていた。POLO 試験の結果より,日本では2020 年12 月に「BRCA 遺伝子変異陽性の治癒切除不能な膵癌における白金系抗悪性腫瘍剤を含む化学療法後の維持療法」としてオラパリブが薬事承認されている。オラパリブの適応を判断するためのコンパニオン診断薬として生殖細胞系列BRCA1/2 病的バリアントの有無を評価するBRACAnalysis 診断システムも同時に承認されている。
本CQ では,プラチナ製剤感受性切除不能BRCA1/2 病的バリアントを保持する膵癌を対象として,PARP 阻害薬単独とプラセボの2 群間で比較した際の「全生存期間(OS)」「無増悪生存期間」「有害事象」「コスト」「患者の意向」「患者の満足度」の6 項目をアウトカムとして設定し,システマティックレビューの評価対象とした。
本CQ に対する文献検索の結果,PubMed 229 編,Cochrane 210 編,医中誌38 編が抽出され,計477 編がスクリーニング対象となった。2 名のシステマティックレビュー委員が独立して計2 回の文献スクリーニングを行い,抽出された8 編がシステマティックレビューの対象となった。
一次治療のプラチナレジメンで16 週以上病状進行が抑えられた,生殖細胞系列BRCA1/2 病的バリアントを保持する転移性膵癌患者を対象とし,オラパリブ維持療法とプラセボを比較するランダム化第Ⅲ相試験(POLO 試験)が行われた5)。OS では両群間で統計学的な有意差を認めなかった〔中央値:18.9 カ月vs. 18.1 カ月,HR:0.91(95%CI:0.56-1.46,P=0.68)〕。しかしこの結果は後治療を受けた患者の割合がオラパリブ群では48.9%であったのに対しプラセボ群は74.2%と多く,さらにプラセボ群では14.5%の患者がPOLO 試験外でPARP 阻害薬の投与を受けていた等の要素も関係していたと考えられる。OS の最終結果においても両群におけるOS に有意差は認めなかった〔中央値:19.0 カ月vs. 19.2 カ月,HR:0.83(95%CI:0.56-1.22,P=0.3487)〕6)が,3 年生存割合はオラパリブ群で33.9%,プラセボ群で17.8%であった2)。
またプラチナレジメンで16 週以上病勢コントロールが得られた切除不能膵癌に対してPARP 阻害薬であるrucaparib(本邦未承認)の有効性を評価した第Ⅱ相試験7)では,OS 中央値が23.5 カ月(95%CI:20-27)であったが,対象に生殖細胞および体細胞系列のPALB2 の病的バリアントも含まれていることから延命効果の評価は困難である。
POLO 試験では無増悪生存期間においてオラパリブ群がプラセボ群と比較し有意な延長を認めた〔中央値:7.4 vs. 3.8 カ月,HR:0.53(95%CI:0.35-0.82)〕5)。Rucaparib の有用性を評価した第Ⅱ相試験では無増悪生存期間中央値が13.1 カ月(95%CI:4.4-21.8)であった7) 。
POLO 試験においてオラパリブ群で報告された主な有害事象は疲労(60%),悪心(45%),貧血(27%)等であり,Grade 3 以上の有害事象発生割合はオラパリブ群で40%,プラセボ群で23%であったが,投与中止を要する有害事象はそれぞれ5%,2%であり,管理可能な安全性プロファイルであった5)。
Rucaparib の有用性を評価した第Ⅱ相試験ではGrade 3 の有害事象として貧血(22%),疲労(4%)等が報告されたが,Grade 4 の治療関連有害事象は認めなかった7)。
以上より,生殖細胞系列BRCA1/2 病的バリアントを保持するプラチナ感受性切除不能膵癌に対してPARP 阻害薬は管理可能と考えられるが,これらの試験には日本人の患者は参加していないことに注意が必要である。
POLO 試験のデータをもとにオラパリブによる維持療法の費用対効果について検討が行われている8)~10)。
いずれの報告も増分費用対効果を使用して評価しているが,1QALY(質調整生存年:Quality-adjusted life year)延長するための費用は13,327~265,290 US ドルと報告に幅があった。さらに欧米と中国での報告のみであり,わが国との医療制度が異なるためこれらの結果を適応することは難しい。
POLO 試験に登録された患者に関するQOL についての報告11)~13)はあるものの,評価方法が異なり患者の意向に関して一定の見解を示すのは困難である。しかしプラセボ群と比較しEORCT QLQ-C30 に有意差はないことが報告されており5)6),オラパリブ維持療法による明らかなQOL 低下をきたさないことが想定されること,管理可能な有害事象プロファイルであることを考慮すると,患者の意向に対してネガティブな影響は少ないと考えられる。
⑤で述べたとおり,オラパリブ維持療法による明らかなQOL 低下をきたさないことが想定されることから,患者の満足度は損なわれないと考える。
POLO 試験5)ではプラチナ製剤感受性転移性生殖細胞系列BRCA1/2 病的バリアントを保持する膵癌に対するオラパリブ維持療法はプラセボと比較し無増悪生存期間を有意に延長した。OS では統計学的に有意差を示せなかったが,3 年生存割合はプラセボ群より良好であった6)。またオラパリブは内服薬で利便性も高く,有害事象も管理可能であり,明らかなQOL 低下は認めないことを考慮すると,同対象に対する治療選択肢が増えるという観点からも臨床的意義は十分にあると考えられる。
POLO 試験においてGrade 3 以上の有害事象発生割合はオラパリブ群で40%,プラセボ群で23%であったが,中止を要する有害事象の発生割合は両群ともに高くはなく,管理可能と考えられる。
コストに関する海外からの報告の結果をわが国におけるオラパリブ維持療法の費用対効果に外挿することは困難である。オラパリブ維持療法によるQOL に関する報告は,評価方法が異なり一定の見解を示しにくいが,QOL を明らかに損なうという報告はなかった。
本CQ の推奨決定会議参加対象委員12 名の内訳は,乳癌領域医師2 名,婦人科領域医師2 名,遺伝領域医師2 名,遺伝看護専門看護師1 名,認定遺伝カウンセラー2 名,患者・市民3 名であった。推奨決定会議の運営にあたっては,事前に資料を供覧し,参加対象委員全員がEvidence to Decision フレームワークを記入して意見を提示したうえで,当日の議論を行った。推奨決定会議には参加対象委員のうち,10 名が参加した。
遺伝性腫瘍のガイドラインで治療法に関するCQ の優先度という観点では優先度がわからない,という意見があったが,最終的なvoting では下記の結果であった。
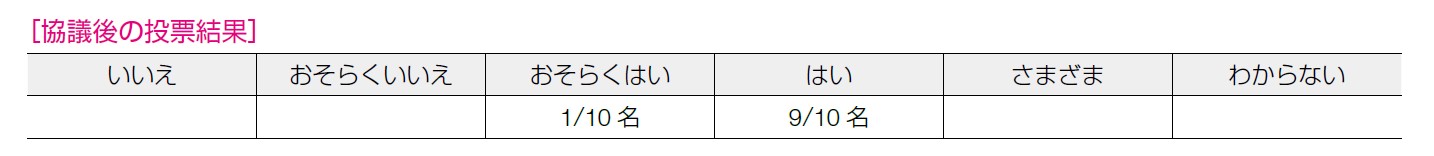
PFS の延長のみ示された点について,クロスオーバーの影響等も加味して,議論された。
また,POLO 試験に日本人が入っていない点も議論された。実際に国際共同試験で日本が参加していてもごく少数例で,有効性のサブ解析では十分な情報になり得ないこともあるが,日本人で毒性プロファイルが異なる可能性もある。膵癌におけるオラパリブについては日本人のブリッジングスタディも行われないまま承認されたが,日常診療で特に日本人に特定の有害事象が多いという情報は今のところは聞いていない。
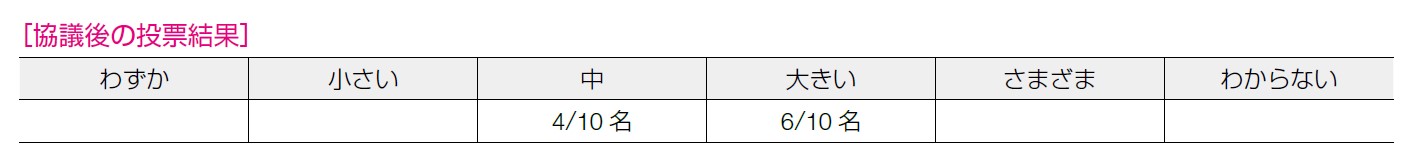
有害事象が40%という点は気になるという声もあった。二次発がんについては大きな問題にならないと考えられた。有害事象については膵癌の進行が速い病状を考えると,無治療は考えにくく,オラパリブを使わない場合の代替としては細胞障害性薬剤での維持療法となることも考慮に入れる必要がある点を共有された。
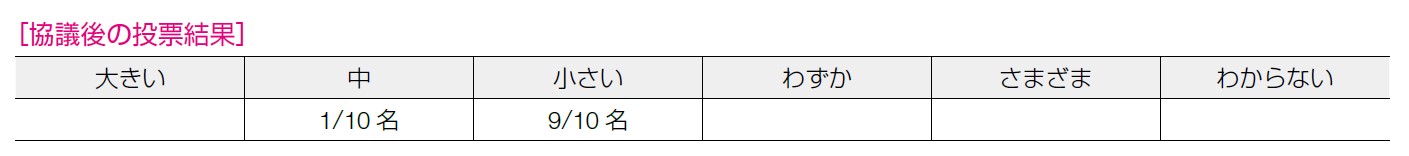
OS の延長効果が示されていない,無増悪生存期間が主要評価項目である,臨床研究としてエビデンスを示すプロセスとしてはランダム化比較試験が行われている,という点で,(少なくとも無増悪生存期間については)エビデンスの確実性は強いと考えられる。OS の延長効果が示されていないことや他のメタ解析等の豊富な情報があるわけではないこと等を総合的に加味すると,「中」と判断した委員 も多かった。

生命予後のみならず,QOL,費用等も加味されるであろうことから,重要な不確実性またはばらつきの可能性もあると考える意見もあった。膵癌診療の現場でも,あくまで無増悪生存期間である,細胞障害性薬剤継続をコントロールとしているわけではない点等もあり,エビデンスの受け取り方への慎重論は確かにある。主要アウトカム(OS,無増悪生存期間,有害事象,コスト)についての価値観のばらつきを「重要な」と判断すべきか,QOL 等も含めたものなのか,等についても質問があがった。主要なアウトカム以外も議論され,配慮されることは問題ない。
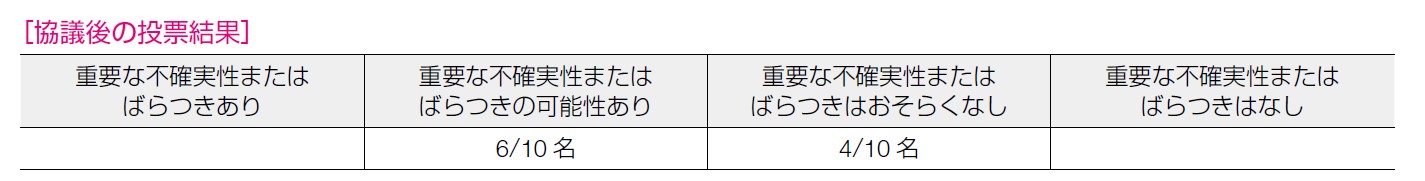
治療選択肢が少ない膵癌で無増悪生存延長効果が有意という点,有害事象が許容範囲であろうこと等からおそらく介入が有意と判断した,といった意見が多かった。

海外では費用対効果の報告が3 編あり。無増悪生存期間においての増分費用効用費(incremental cost-utility ratio:ICUR)が算出されており,費用対効果ありが2 編,なしが1 編あった。ただし,プラセボと比較した場合の話である。日常診療では細胞障害性薬剤継続との比較になる点等も考慮の必要がある。

QOL について特に下げていないという情報も含め,容認性はある,もしくはおそらくある,という意見であった。
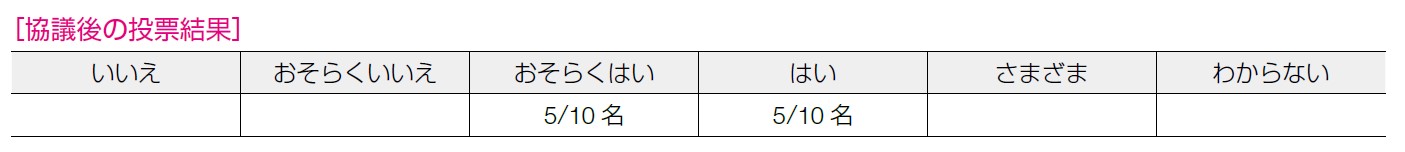
遺伝診療との協力体制が必要な点などから「おそらくはい」を選択したという意見もみられた。膵癌領域でも遺伝性疾患の診療の重要性について広く認知されてきているという情報共有も行われた。
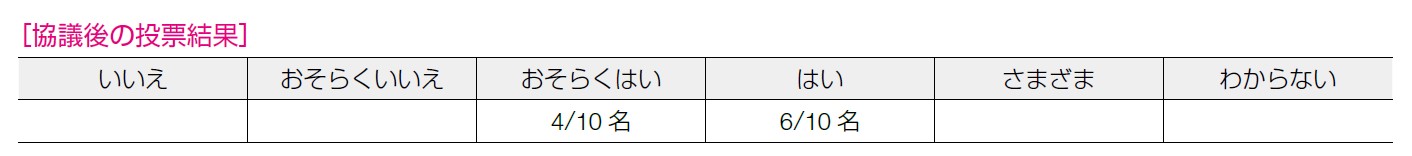
遺伝外来が重要な案件はすべて(遺伝外来に関する)条件付きの・・とするのか,特に薬剤の推奨度は高いが,遺伝外来への紹介が条件,という場合には「条件付きの推奨」とするのか,という点が議論された。この点はガイドライン全体のポリシーとして議論を続けるとして,膵癌では細胞傷害性薬剤を継続する維持療法も選択肢になり得る中,プラセボコントロールでのエビデンスである点等もあり,薬剤の推奨度自体も含め,条件付き,という点はいずれにしても妥当なのではないか,という意見もあった。

膵癌診療ガイドライン14)では,CQ「生殖細胞系列BRCA1/2 の病的バリアントを保有する膵癌に対して化学療法は何が推奨されるか?」に対し,下記のステートメントが提示されている。
NCCN ガイドライン15)ではMetastatic Disease(Maintenance Therapy)の中で,プラチナベースの化学療法の維持化学療法としてOlaparib がonly for germline BRCA1/2 mutations という但し書きのうえで,preferred regimens の欄に明記されている。
ESMO*ガイドラインでは下記の記載がなされている。Olaparib maintenance treatment is an option for patients with a gBRCA1/2 variant whose disease is stable or responsive to platinum-based ChT[I, B;ESMOMCBS v1.1 score:2;ESMO Scale for Clinical Actionability of molecular Targets(ESCAT)score:I-A]
ESMO:European Society for Medical Oncology
オラパリブがOS の延長に寄与しているか,についてはPOLO 試験では示されていないため,今後評価が望まれる課題である。また,POLO 試験で示されたのはプラチナレジメン後の維持療法としての治療効果であるが,維持療法としてではなく,PARP 阻害薬自体の治療薬としての有効性についても今後の課題といえる。また,膵癌におけるPARP 阻害薬の耐性機序,耐性克服のための治療法開発等も今後の課題である。
今回のシステマティックレビューの結果では,生殖細胞系列BRCA1/2 病的バリアントを保持するプラチナ感受性切除不能膵癌に対する維持療法としてのPARP 阻害薬の「OS」に関する報告は限定的だった。また,POLO 試験に日本人が参加していない点,費用対効果についても複数の報告はあるが欧米と中国での報告のみであり,わが国との医療制度が異なるため結果を適応することは難しいことから日本人の情報は限定的と考えられた。この点に関しはさらなるモニタリングが必要と思われる。患者(利用者)に対する遺伝外来への案内や実施施設に関する情報整備,臨床医の遺伝性腫瘍にまつわる適切な対応方法の習得も必要と思われる。
外部評価では内容に関する大きな指摘はなかった。
BRCA,gene mutation,pancreatic cancer,parp inhibitor,Platinum Sensitivity,chemotherapy,FOLFIRINOX,patient preference,patient satisfaction,cost
文献検索式,エビデンス総体評価シート,システマティックレビューレポート,Evidence to Decisionフレームワークは,JOHBOC ホームページに掲載。
