Ⅱ-3 卵巣癌領域
乳癌未発症のBRCA1/2 病的バリアント保持者に対し,HRT を条件付きで推奨する。
推奨のタイプ:当該介入の条件付きの推奨
エビデンスの確実性:弱,合意率:91.6%(11/12 名)
推奨の解説:乳癌未発症のBRCA1/2 病的バリアント保持者に対するHRT により,乳癌,卵巣癌,子宮内膜癌の発症率が上昇するという強いエビデンスはなく,更年期症状や骨粗鬆症等,エストロゲン低下による諸症状を緩和する等の目的でHRT を行うことは許容できる。しかしながら,長期投与による乳癌発症リスクやBRCA1 または2 での乳癌発症率の違いについては不確かさが残る。また,リスク低減卵管卵巣摘出術(RRSO)実施の有無によっても乳癌発症リスクは異なる。乳癌未発症のBRCA1/2 病的バリアント保持者に対し,HRT を施行するメリット・デメリットを話し合い,乳癌サーベイランスや遺伝診療部・遺伝カウンセラーの連携が実施できる施設かつ女性ヘルスケアに精通した専門医のもとHRT を行うことを条件付きで推奨する。
BRCA1/2 病的バリアント保持者にはRRSO が推奨される。RRSO は外科的閉経を起こしエストロゲン低下による血管運動神経障害症状,心血管疾患,脂質代謝異常,認知機能低下,骨粗鬆症,性機能低下などの諸症状を惹起しQOL を低下させる。外科的閉経女性は自然閉経女性よりも生存期間が短い1)。そこでRRSO により低下したエストロゲンを補うHRT が考慮される。エストロゲン単独療法あるいはエストロゲン+プロゲスチン併用療法が乳癌リスクにどのような影響を及ぼすのかも重要な課題である。RRSO 後にHRT を行っても乳癌発症のリスクは上昇しない2)。また,RRSO を行わずサーベイランスを行うBRCA1/2 病的バリアント保持者の女性にも周閉経期の諸症状にHRT が施行される。BRCA1 病的バリアント保持者のRRSO 未施行例でのHRT 使用は4.3 年までの観察で乳癌発症を増加させない3)。一方,BRCA2 病的バリアント保持者のRRSO 未施行例でのHRT の安全性に関するデータはない。一般集団でのコホート研究では,エストロゲン単独療法では13 年間の観察中乳癌の発症リスクを増加させないが,エストロゲン+プロゲスチン併用療法では5 年未満の使用であれば有意差はないが5 年を越すと乳癌発症のリスクが増加する4)。したがってHRT,特にエストロゲン+プロゲスチン療法は5 年を超えない短期間の使用が望ましい。乳癌既往者に対するHRT は再発,転移,対側乳癌発症を6.9 倍増加させることからHRT は禁忌とされているため5),諸症状に対して対症療法が選択されている。BRCA1/2 病的バリアント保持者女性に対するHRT のベネフィットとリスクを検討する。
本CQ では,乳癌未発症のBRCA1/2 病的バリアント保持者を対象として,HRT を実施した群と実施しなかった群の2 群間で比較した際の「乳癌発症リスク」「OS」「有害事象」「費用対効果」「患者の満足度」の5 項目をアウトカムとして設定し,システマティックレビューの評価対象とした。
本CQ に対する文献検索の結果,PubMed 140 編,Cochrane 3 編,医中誌12 編が抽出され,これにハンドサーチ1 編を加えた計156 編がスクリーニング対象となった。2 名のシステマティックレビュー委員が独立して計2 回の文献スクリーニングを行い,抽出された14 編がシステマティックレビューの対象となった。
現在までに乳癌発症リスクについて,メタ解析1 編とコホート研究3 編,症例対象研究3 編で評価されている。RRSO 後のBRCA1/2 病的バリアント保持者におけるHRT の使用を検討したランダム化比較試験はない。
Rebbeck らによるコホート研究では,BRCA1/2 病的バリアント保持者462 例を平均3.6 年間追跡し,HRT による乳癌リスクを評価した2)。このコホートでは,155 例の女性が平均42.7 歳でRRSO を施行し,93 例がHRT を使用した。RRSO は有意に乳癌リスクを低下させ〔HR:0.40(95%CI:0.18-0.92)〕,このリスク低下はHRT の使用による影響を受けなかった〔HR:0.37(95%CI:0.14-0.96)〕。HRT の薬剤は,50 例がエストロゲン単独療法(estrogen therapy:ET)を受け,34 例がエストロゲン・黄体ホルモン併用療法(estrogen progestin therapy:EPT)を受けたが,両者で乳癌リスクに差は確認されなかった。
Eisen らは,未閉経のBRCA1 病的バリアント保持者473 例(236 組)を対象とした症例対象研究を実施した6)。HRT の平均使用期間は症例群で3.7 年間,対象群で4 年間であった。HRT 使用は乳癌リスク低下と関連した〔OR:0.58(95%CI:0.35-0.96)〕。また薬剤別では,ET で有意なリスク低下〔OR:0.51(95%CI:0.27-0.98)〕を認めた一方,EPT では統計的に有意ではないリスク低下〔OR:0.66(95%CI:0.34-1.27)〕を示した。この研究の延長がKotsopoulos らによって行われ,BRCA1 病的バリアント保持者864 例(432 組)の症例対象研究として報告された3)。HRT 使用者は症例群で91 例(21%),症例群で80 例(19%)と同程度であった(P=0.24)。HRT 使用の平均期間は,症例群で4.42 年,対象群で4.27 年であった。結果として,乳癌リスクとHRT 使用との間に関連は認められなかった〔OR:0.80(95%CI:0.55-1.16)〕。ET が症例群で46 例,対象群で42 例,EPT が症例群で28 例,対象群で41 例であったが,ET,EPT いずれの製剤でも乳癌のリスク増減とは関連しなかった〔ET はOR:1.00(95%CI:0.62-1.62),EPT はOR:0.65(95%CI:0.38-1.11)〕。閉経のタイプ(自然閉経327 組vs. 外科的閉経105 組)を分けて検討しても有意差は観察されなかった〔自然閉経はOR:0.72(95%CI:0.44-1.18)〕,外科的閉経はOR:1.06(95%CI:0.44-1.18)〕。
Kotsopoulos らは続いてRRSO を施行した872 例のBRCA1 病的バリアント保持者を対象としたコホート研究も報告しているが7),そのサブセットは前述の症例対象研究と重複している。RRSO 後にHRT を使用した377 例と使用しなかった495 例を追跡した結果,RRSO 後のHRT は乳癌リスクの上昇とは関連しないことが示された〔HR:0.97(95%CI:0.62-1.52)〕。10 年間の追跡後,EPT 使用群と比較してET 使用群の乳癌リスクが有意に低いことも観察された(ET 12% vs. EPT 22%,P=0.04)。その関連は45 歳未満でRRSO を受けた症例でより顕著であった。
さらにMichaelson-Cohen らは,RRSO 施行後に平均7.26 年追跡された306 例のBRCA1/2 病的バリアント保持者を対象とした症例対象研究を報告した8)。HRT 群148 例と非HRT 群155 例を比較した結果,RRSO 施行時に45 歳以下であった症例では,HRT は乳癌リスクを増加させないことが示された〔OR:0.8(95%CI:0.3-1.9)〕。一方で,45 歳以上でRRSO を施行しHRT を使用した症例では乳癌リスクが有意に高かった〔OR:3.43(95%CI:1.2-9.8)〕。乳癌発生率にHRT 製剤による有意差は認められなかったが,HRT 使用者の大多数がEPT を受けていた。
メタ解析は一編のみ報告がある9)。計1,100 例を対象とした3 つの研究2)7)10)が解析に含まれた。その結果,RRSO 後にHRT を受けたBRCA1/2 病的バリアント保持者では乳癌発症スクは有意に高くはなかった〔HR:0.98(95%CI:0.63-1.512)〕。ET とEPT の比較ではわずかであるが有意ではないものの,乳癌リスク減少の有益性が認められた〔OR:0.53(95%CI:0.25-1.15)〕。結論として,HRT 使用は乳癌発症リスクに影響しないことが示唆され,HRT 製剤としては子宮を保持していない女性にはET が最も安全で合理的な選択であるとしている。
以上の研究を総合すると,乳癌既往のないBRCA1/2 病的バリアント保持者に対する,3~5 年の短期的なHRT の使用は乳癌の増加とは関連しないことが示唆される11)~14)。
最後に11 カ国(米国,カナダ,英国,オーストラリア,ノルウェー,フィンランド,デンマーク,ドイツ,フランス,ポルトガル,オランダ)の2009~2016 年に発表されたガイドラインにおけるRRSO後のHRT の取り扱いについて分析したレビューを紹介する13)。ポルトガル以外のすべてのガイドラインで,乳癌既往のない閉経前女性に対する短期のHRT 使用は安全と考えられていた。ポルトガルのガイドラインでのみ,BRCA1/2 病的バリアント保持者にHRT を使用しないことを推奨しているが,一部の選択された症例では考慮してもよいとしている。同ガイドラインがその結論を導いた理由は不明である。ほとんどのガイドラインで短期使用は自然閉経の平均年齢までとしている。
RRSO による早期外科的閉経後のBRCA1/2 病的バリアント保持者に対する短期的HRT 使用が乳癌発症リスクを増加させないことを示唆する質の高い観察研究が数多く存在するが,ランダム化比較試験がないことから,今回のシステマティックレビューでは,エビデンスの強さはC(弱)とした。
採用研究はなかった。
採用研究はなかった。
採用研究はなかった。
採用研究はなかった。
本システマティックビューにおいては,患者の満足度を更年期症状の改善,性機能の改善,骨粗鬆症予防の3 点において評価することとし,既存のシステマティックビュー4 編を採用した15)~18)。更年期症状については主にホットフラッシュが中心となり,改善が示されている15)~18)。性機能については,不快感と疼痛,腟の乾燥等がHRT により改善されると報告されている16)18)。骨についても,HRTの内容や投与期間が不明で,HRT による骨量の変化値を客観的に評価することは困難だが,骨量減量の予防や骨折リスク減少の効果が認められている16)~18)。すなわち,BRCA1/2 病的バリアント保持者に対するHRT により,種々の更年期症状や性機能の改善,骨粗鬆症リスクの低減が期待される。
ただし,更年期症状や性機能の改善を図る尺度としてはFACT-ES,MSL,MENQOL,MRS,SAQ,FSFI,FSDS 等の様々なツールが使用されていることや,RRSO を受けた年齢,閉経年齢,HRT の投与期間や投与薬剤,投与経路等が報告によって異なっていること,またその特性上アウトカムの評価がアンケートや聞き取り調査的なものにならざるを得ないことには注意が必要であることから,エビデンスの強さは中とした。
BRCA1/2 病的バリアント保持者に対し,HRT を行うことで得られる更年期症状や性機能の改善,骨粗鬆症の予防といったベネフィット/QOL については,一貫して改善することが示されている。基本的,理論的には,HRT によるこれらのQOL 改善はBRCA1/2 病的バリアントの有無にかかわらず得られると考えられ,必要時にはその実施を考慮すべきである。
乳癌既往のないBRCA1/2 病的バリアント保持者に対する,3~5 年の短期的なHRT の使用は乳癌の増加とは関連しないことが示唆される。ただし次の3 点に注意を要する。①RRSO 後のBRCA1/BRCA2 病的バリアント保持者におけるHRT 使用を評価した観察研究は多数存在するが,報告されている使用期間には幅があること(平均3.6~7.6 年)から,同集団に対する5 年以上の長期的なHRT の影響についてはさらなる調査を要する。②また一部の報告ではEPT 使用に関連したリスク増加が観察されたが,一方ではET とEPT のいずれも乳癌リスク増加に関連しないとする報告も多く存在する。製剤の違いによる関連についてもさらなる検討が必要である。③上記既報の対象症例の大多数はBRCA1 病的バリアント保持者であり,BRCA2 病的バリアント保持者におけるHRT に関するデータが比較的乏しいことにも留意すべきである。
将来的にはより大規模なランダム化比較試験が行われることが望まれる。
本CQ の推奨決定会議参加対象委員12 名の内訳は,乳癌領域医師2 名,婦人科領域医師2 名,遺伝領域医師2 名,遺伝看護専門看護師1 名,認定遺伝カウンセラー2 名,患者・市民3 名であった。推奨決定会議の運営にあたっては,事前に資料を供覧し,参加対象委員全員がEvidence to Decision フレームワークを記入して意見を提示したうえで,当日の議論を行った。推奨決定会議には参加対象委員全員が参加した。
現在までに乳癌発症リスクについて,メタ解析1 編とコホート研究3 編,症例対象研究3 編で評価されている。RRSO 後のBRCA1/2 病的バリアント保持者におけるHRT の使用を検討したランダム化比較試験はない。
RRSO による早期外科的閉経後のBRCA1/2 病的バリアント保持者に対する短期的HRT 使用が乳癌発症リスクを増加させないことを示唆する質の高い観察研究が数多く存在する。しかし,ランダム化比較試験が存在しないことは懸念材料である。
3 つの研究から1,100 例を対象としたメタ解析では,RRSO 後にHRT を受けたBRCA1/2 病的バリアント保持者では乳癌発症リスクは増加していなかった〔HR:0.98(95%CI:0.63-1.512)〕。ET とEPT の比較では有意ではないものの,わずかであるが乳癌リスク減少の有益性が認められた〔OR:0.53(95%CI:0.25-1.15)〕。結論として,HRT 使用は乳癌発症リスクに影響しないことが示唆される。
推奨決定会議では,「はい」が12 票であった。
外科的閉経患者は高血圧,脂質異常症を早期に発症し,心血管系疾患の罹患率が増加する。また骨粗鬆症の発症が有意に高い。したがって,外科的閉経患者にHRT を施行しない場合,寿命は短くなることが証明されている。また,外科的閉経患者の更年期症状は強くさらに性機能に悪影響を及ぼしQOL の面から不利益を被ることが多い。RRSO 施行患者は外科的閉経が多いため,乳癌未発症のBRCA1/2 病的バリアント保持者にHRT を行うことの安全性を担保できるかどうかは重要な問題である。
望ましい効果として,HRT を行うことで更年期症状や性機能の改善,骨粗鬆症の予防といったベネフィット/QOL への有効性である報告は一貫している。
推奨決定会議では,「大きい」が7 票,「中」が5 票であった。
基本的,理論的には,HRT によるこれらのQOL 改善はBRCA1/2 病的バリアントの有無にかかわらず得られると考えられ,HRT が必要なときはその実施を考慮すべきである。

報告されているHRT 使用期間には幅があること(平均3.6~7.6 年)から,同集団に対する5 年以上の長期的なHRT の影響についてはさらなる調査を要する。プロゲスチン製剤の違いによる発がんリスクについてもさらなる検討が必要である。BRCA2 病的バリアント保持者におけるHRT に関するデータが比較的乏しい。
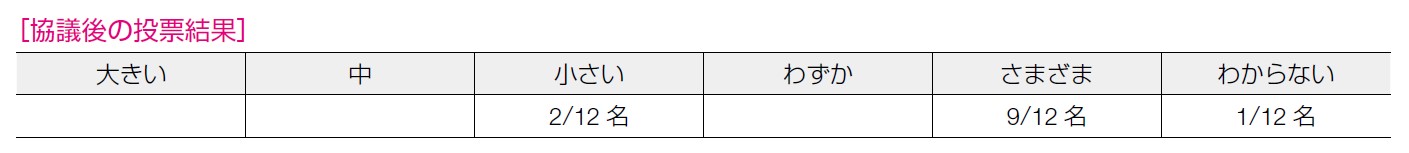
推奨決定会議では,システマティックレビューからHBOC に関して特有のHRT リスクが上がることの記載がないこと,3~5 年の短期的な範囲での乳癌リスク上昇はないというエビデンスはあるが,より長期のものがないこと,ランダム化比較試験の結果ではないため,バイアスがないかどうかの注意が必要であること,エストロゲン単独投与が乳癌低減効果につながるという報告も出てきているため,最新のエビデンスを反映する必要があること,エビデンスではリスク低減乳房切除術(risk reducing mastectomy:RRM)を行った群が含まれているかについて記載はなく乳癌発症者が含まれている可能性があること,という多様な意見が出て,介入の望ましくない効果は「さまざま」が9 票となった。「小さい」は2 票,「わからない」は1 票であった。
HRT の使用期間,投与量,製剤の選択や,BRCA2 病的バリアント保持者におけるHRT の安全性についての情報はまだ十分ではないことに留意する必要がある。
今回のシステマティックレビューではランダム化比較試験による報告はなく,メタ解析も含め,後方視的解析である。しかし,どの研究も,HRT は乳癌の発症リスクを増加させない,ということで一致している。
今回のシステマティックレビューではアジア圏の報告がないため,人種差の影響については不明であることに注意を要する。がん種は違うが,子宮内膜癌術後のHRT は,再発を増加させないということでコンセンサスが得られているが,黒人に限り解析すると,HRT の使用により再発リスクが約7倍に増加することが報告されている。
アジア圏,特に日本人の乳癌未発症のBRCA1/BRCA2 病的バリアント保持者にHRT を行ったまとまったデータがないことが懸念材料である。
したがって,推奨決定会議では,「弱」が11 票,「中」が1 票であった。

HRT の患者満足度を更年期症状の改善,性機能の改善,骨粗鬆症予防の3 点において評価した。更年期症状については主にホットフラッシュが中心となり,改善が示されている。性機能については,不快感と疼痛,腟の乾燥等がHRT により改善されると報告されている。骨についても,HRT による骨量減量の予防や骨折リスク減少の効果が認められている。すなわち,BRCA1/2 病的バリアント保持者に対するHRT により,種々の更年期症状や性機能の改善,骨粗鬆症リスクの低減が期待される。
しかし,更年期症状や性機能の改善を図る尺度としてはFACT-ES,MSL,MENQOL,MRS,SAQ,FSFI,FSDS 等の様々なツールが使用されていることや,RRSO を受けた年齢,閉経年齢,HRT の投与期間や投与薬剤,投与経路等が報告によって異なっていること,またその特性上アウトカムの評価がアンケートや聞き取り調査的なものにならざるを得ないことには注意が必要である。
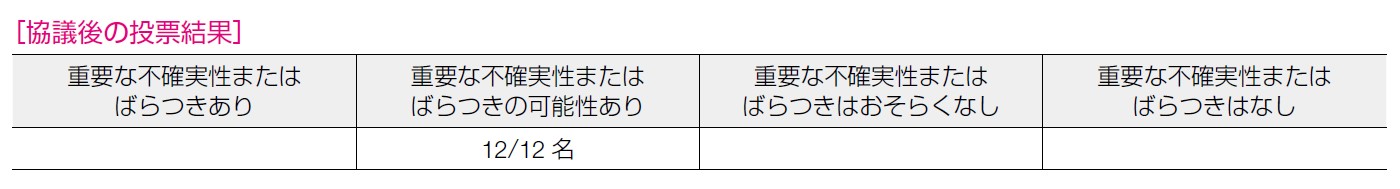
したがって,推奨決定会議では,「重要な不確実性またはばらつきの可能性あり」が12 票であった。
HRT によっても乳癌発症リスクは上昇しない,RRSO 後のHRT により更年期症状の改善,骨粗鬆症予防,性機能低下が改善するという一貫したリサーチエビデンス結果からHRT 介入が優位である。
理想的なHRT の使用期間,投与量,製剤の選択(ET vs. EPT)や,BRCA2 病的バリアント保持者におけるHRT の安全性についての情報はまだ十分ではないことに留意する必要がある。繰り返しになるが人種差のエビデンスがない。
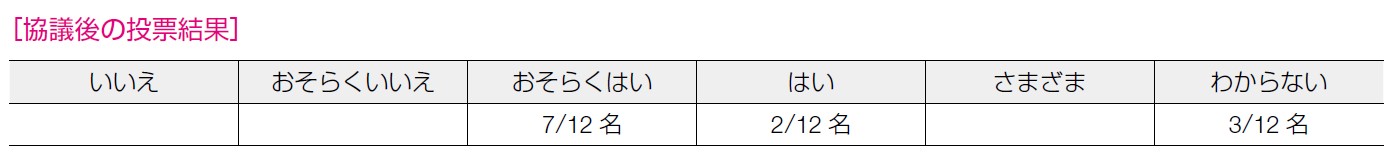
推奨決定会議では,乳癌未発症,更年期症状がつらいということであれば,選択肢としてHRT は提示してよい。しかし,エビデンスのベースとなる論文にRRM 群が含まれている,また乳癌既発症が含まれていると判断が難しくなってくる。対象集団に様々な背景がある可能性があり,ET をするのかEPT をするのかで判断が難しくなる,という意見が出た。そのような意見を反映してか,「おそらく介入が優位」5 票,「介入が優位」1 票,「さまざま」6 票であった。

採用研究なし。

乳癌未発症者のBRCA1/2 病的バリアント保持者に対するHRT は長期でなければ容認性は高い。費用負担について,内服薬や貼付剤,ジェル等がある。プレマリンは1 カ月で340 円前後,ジェルや貼付剤は1 カ月1,000 円弱である。
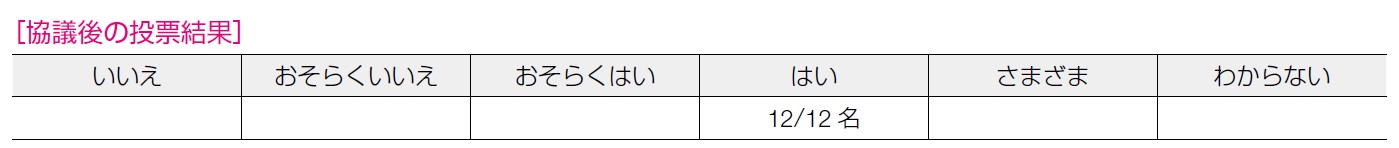
推奨決定会議では,更年期症状を抑える手段として漢方だけ提示されたが,HRT も選択肢だったのであれば試してみたかったという意見があった。投票では,「おそらくはい」が7 票,「はい」が2 票,「わからない」が3 票であった。
実行可能性については,通常の保険診療の範囲内で実施可能である。エビデンス総体からも5 年未満の短期のHRT の介入は実行可能である。
推奨決定会議では,投与期間がどこまでかという不確定要素があるという懸念があげられた。また,婦人科と乳腺外科でガイドライン上でも意思統一を図ること,対象者の意思決定を支援できる医療者(臨床遺伝専門医,遺伝カウンセラー,遺伝看護専門看護師等)が関わり,患者さんの意思決定をサポートすることが重要であること,アウトカムとして女性のヘルスケアの改善が最も重要で,乳癌リスクはその副作用として考えてもよいのではないか,という意見があった。乳癌未発症者でも,RRSOでの卵巣欠落症状としてのHRT は保険診療として行えることが確認された。投票では「おそらくはい」が8 票,「はい」が4 票であった。

以上より,乳癌未発症のBRCA1/2 病的バリアント保持者に対し,HRT は推奨されるかについて討議し条件付きの推奨となった。乳癌サーベイランスが実施できる施設,女性ヘルスケアに精通した専門医,対象者の意思決定を支援できる医療者(臨床遺伝専門医,遺伝カウンセラー,遺伝看護専門看護師等)の連携のもとで実施する,患者さんとよく話し合いをして決定するという文言を入れるべきという意見があった。このような条件付きで11/12 名(91.7%)で採用が決定した。
また,推奨決定会議では,HRT 使用後にある一定数乳癌発症者が出てくるが,HRT という介入が発症に影響したかを答えられるような文言が必要であるということ,HRT を行うことが乳癌リスク的に許容される群を抽出することはできないだろうかという意見が出た。

「ホルモン補充療法ガイドライン19)で「BRCA1/2 遺伝子変異陽性女性に対するHRT は可能か?」というCQ に対して,短期の投与は可能である(推奨レベル1,エビデンスレベル+++-)と記載されている。
今回のエビデンスはランダム化比較試験による報告はなく,メタ解析も含め,後方視的解析であることに留意が必要である。また今回のシステマティックレビューではアジア圏の報告がないため,人種差の影響については不明であるためこの点についてさらなるエビデンスの集積が待たれる。また,理想的なHRT の使用期間,投与量,製剤の選択(ET vs. EPT)や,BRCA2 病的バリアント保持者におけるHRT の安全性についての情報はまだ十分ではないことに留意する必要がある。
特になし。
外部評価では内容に関する大きな指摘はなかった。
BRCA,HRT,side effect,cost,patient preference,QOL,breast cancer
文献検索式,エビデンス総体評価シート,システマティックレビューレポート,Evidence to Decisionフレームワークは,JOHBOC ホームページに掲載。
