Ⅱ-2 乳癌領域
BRCA1/2 病的バリアントを保持する乳癌患者に対し,新規乳癌発症予防のためにタモキシフェン(TAM)を投与することを条件付きで推奨する。
推奨のタイプ:当該介入の条件付きの推奨
エビデンスの確実性:弱,合意率:100%(11/11 名)
推奨の解説: システマティックレビューで参照したメタ解析の結果から,TAM 内服による対側乳癌予防の確実性は「弱」であるといえる。その一方で,有害事象については子宮内膜癌の発症に注意が必要であるものの望ましくない効果については中等度といえる。患者の価値観についての研究は存在しないものの,重要な不確実性またはばらつきの可能性ありと判断されており,実施にあたっては患者と医療者による協働意思決定が重要である。TAM は乳癌の術後治療として保険診療での処方が可能であるが,予防を目的とする投与については保険適用外であることに留意が必要である。
BRCA1/2 病的バリアントを保持する乳癌患者において,新規乳癌(対側乳癌)の発症が,BRCA1/2 病的バリアントを保持しない場合と比較して多いことが示されている。タモキシフェン(TAM)はホルモン受容体陽性乳癌では術後内分泌療法として確立した治療ではあるが,新規乳癌発症予防に特化した効果やホルモン受容体陰性乳癌での治療効果は明らかとなっておらず,対象患者において新規乳癌発症予防を目的として内服することの意義については検討の余地がある。このCQ が明らかとなることにより,特にホルモン受容体陰性乳癌で新規乳癌発症予防を目的としてTAM を内服すべきかどうかについての治療選択に有用である。
本CQ ではTAM 内服群と非内服群の2 群間で,「新規乳癌発症リスク(対側乳癌)」「全生存率」「有害事象」「費用対効果」「患者の意向」「患者の満足度」を評価した。
1 編のコホート研究と4 編の症例対照研究,これらのうち4 編を用いたメタ解析を選択した。またBRCA1/2 病的バリアント保持者に限定せずに未発症者を対象として実施されたランダム化比較試験2 編を「有害事象」の評価として採用した。システマティックレビューは,正しい文献検索ストラテジー(search strategy)で論文が選定されており,システマティックレビューチームが2 次スクリーニングで抽出した論文が4 編含まれていた。また,この論文以降に新しい報告がなく,このメタ解析の結果を採用することとした。
メタ解析ではTAM 内服により対側乳癌発症リスクは44%減少した1)。BRCA1/2 のいずれの病的バリアントでも有効性は同等であった。研究の異質性,研究数が少ないこと,すべてが観察研究であることからエビデンスの確実性は弱とした。
【エビデンスの確実性:弱】
全生存率について検討した研究は存在しなかった。
【エビデンスの確実性:該当論文なし】
BRCA1/2 病的バリアント保持者のみを対象としていない2 編の観察研究が参照された2)3)。各有害事象の発症頻度は高くないものの,心血管イベント,子宮内膜癌の発症リスクが上昇することが示された。特にTAM を予防的に内服する場合,子宮内膜癌の増加が問題となるが,その発症頻度は増加するものの絶対数が少なく,望ましくない効果の程度としては中と判断した。研究の異質性,研究数が少ないこと,すべてが観察研究であることからエビデンスの確実性は弱とした。
【エビデンスの確実性:弱】
費用対効果について検討した研究は存在しなかった。
【エビデンスの確実性:該当論文なし】
患者の意向について検討した研究は存在しなかった。
【エビデンスの確実性:該当論文なし】
患者の満足度について検討した研究は存在しなかった。
【エビデンスの確実性:該当論文なし】
乳癌発症リスク(対側乳癌)について,4 編の後ろ向き観察研究と,これらをメタ解析した1 編が採用された1)4)~7)。BRCA1 およびBRCA2 病的バリアントを保持する患者群においてもTAM による予防効果は認められた。Metcalf らによるとBRCA1 よりもBRCA2 でHR:0.73(95%CI:0.4-1.15)で予防効果が高い傾向があるという報告5)もあり,その生物学的特徴からもBRCA1 とBRCA2 は個別に検討される必要性も示唆されたため分離したものも記載した。
さらにGronwald らの報告8)では,従来のピボタル臨床試験(pivotal clinical trial)の報告とは異なり短期間のTAM 投与のほうが予防効果が高いとの結論になっており,その内容の解釈や臨床への適応は十分な検討が必要と考える。
有害事象について,2 編の論文が参照された。いずれもBRCA1/2 病的バリアントを保持する患者のみを対象とした試験ではない。Fisher らの論文2)では骨折の発症は32%減少し〔RR:0.68(95%CI:0.51-0.92)〕,脳梗塞(RR:1.42),深部静脈血栓症(deep venous thrombosis:DVT)(RR:1.44),白内障(RR:1.21),虚血性心疾患(RR:0.91),肺塞栓症(RR:2.15)の発症率は既報と同等であった。子宮内膜癌はTAM によるリスク増加を認めた〔RR:3.28(95%CI:1.82-6.03)〕。Cuzick らの論文3)においてプラセボと比較した各有害事象のOR(95%CI)は,血栓症〔深部静脈血栓症1.72(1.07-2.85),肺塞栓症1.37(0.76-2.49),表在性血栓性静脈炎1.70(1.22-2.37)〕,心血管イベント〔心筋梗塞0.76(0.24-1.67),狭心症1.18(0.72-1.17)〕,脳血管イベント〔脳梗塞/脳血管発作1.07(0.62-1.86),一過性脳虚血発作0.67(0.40-1.12)〕。子宮内膜癌は全体では1.45(0.79-2.71,P=0.19)とTAM 群で多い傾向にとどまる,一方で子宮内膜癌による死亡はTAM vs. プラセボで5 vs. 9 と頻度が高く,既報(1.9 vs. 1.1 per 10 000 women-years)9)と同様であり注意を要する。
本CQ の推奨決定会議参加対象委員12 名の内訳は,乳癌領域医師2 名,婦人科領域医師2 名,遺伝領域医師2 名,遺伝看護専門看護師1 名,認定遺伝カウンセラー2 名,患者・市民3 名であった。推奨決定会議の運営にあたっては,事前に資料を供覧し,参加対象委員全員がEvidence to Decision フレームワークを記入して意見を提示したうえで,当日の議論を行った。推奨決定会議には参加対象委員のうち,11 名が参加した。
委員の意見は「おそらくはい」もしくは「はい」であった。議論の中で,TAM による乳癌発症率低減効果の有無はリスク低減手術,乳房サーベイランスに次ぐ第三の乳房マネージメント法として重要であるとの指摘がなされた。リスク低減手術よりも当事者にとって取り入れやすい治療法であるとの指摘もなされ,参加者全員がリスク低減手術が優先されるものの,他の選択肢として重要であるとの認識をもった。
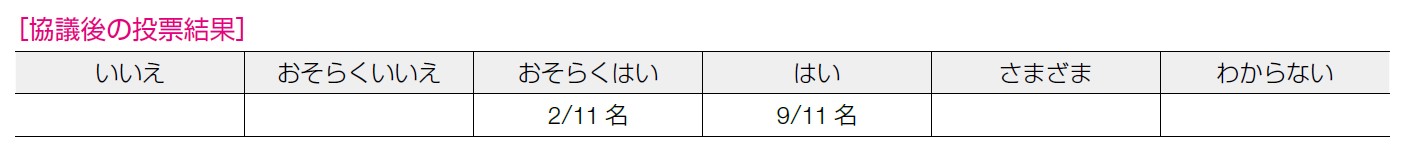
望ましい効果が大きいと考える委員が多い一方,中等度であるとの意見も少なくなかった。TAMの内服によりMRI サーベイランスが不要になるか等,他のマネージメントの代替になるかが不明であるとの指摘がなされた。投与期間について確立されていないこと,RRM という確実性の高い治療があることの指摘がなされた。その一方,予防効果が高いことが示されているので望ましい効果は大きいと判断するとの意見が出された。今後はBRCA1/2 による効果の違いや,投与量,期間について検証すべきとの認識が共有された。

TAM はすでに乳癌治療薬として広く使われており,望ましくない効果としては「中」が大勢を占めた。有害事象が起きることは確かであり,頻度は高くないものの子宮内膜癌等,リスクの高い有害事象もあることが指摘された。

メタ解析が1 報存在するものの観察研究を用いたものであり,エビデンスの確実性は「弱」で全委員の認識が共通であった。本CQ に対する研究が少ないことが共有された。
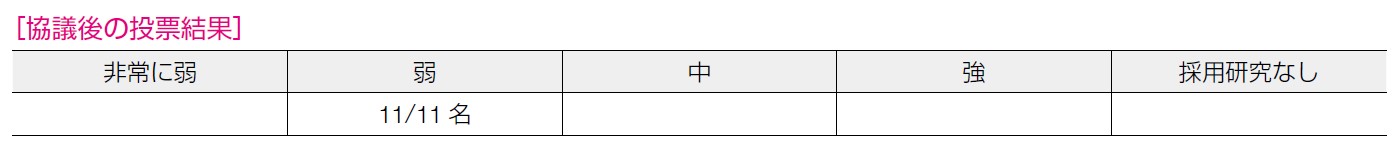
患者の価値観については「重要な不確実性またはばらつきの可能性あり」が多数を占めた。RRM 希望の有無によってTAM に対する価値観はことなると予測されることが指摘された。データが少なく価値観への判断はばらつきが生じる可能性があるものの,メタ解析があること,内服薬であり当事者には参加しやすい治療であることが指摘された。
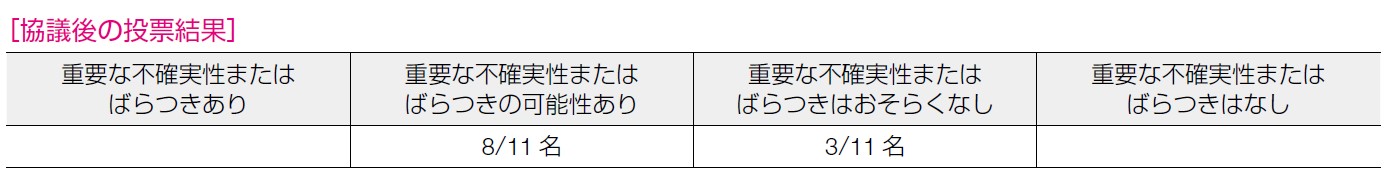
「おそらく介入が優位」で全員が一致した。BRCA2 における発症予防の根拠が強いこと,RRM を希望しない場合に発症予防につながることから,「おそらく介入が優位」であるとの指摘がなされた。一方で,日本人のエビデンスがないことが指摘された。

費用対効果についての採用研究がないことが共有された。

容認性は全員が「おそらくはい」と回答した。費用は安価で全国で入手可能,有害事象についても予測可能なものが多いため容認性が高いことが指摘された。一方で,至適投与期間や投与量について確立していないことが改めて指摘された。
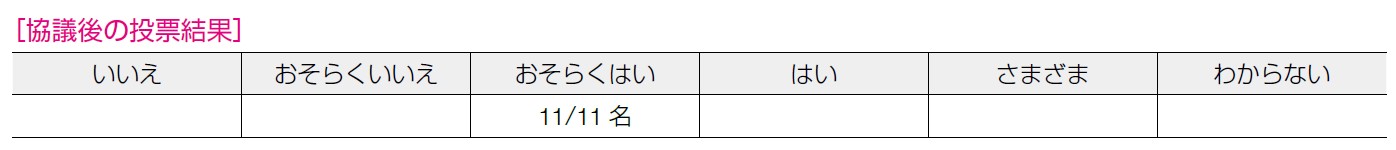
実行可能性は「おそらくはい」ならびに「はい」が選択された。TAM は乳癌を適応症として承認されている薬剤であることから,乳癌術後治療としての投与は保険診療内で実施されるため実行可能性は高いと考えられた。その一方で,予防を目的としての処方は保険適用外となることに注意が必要であることが指摘された。
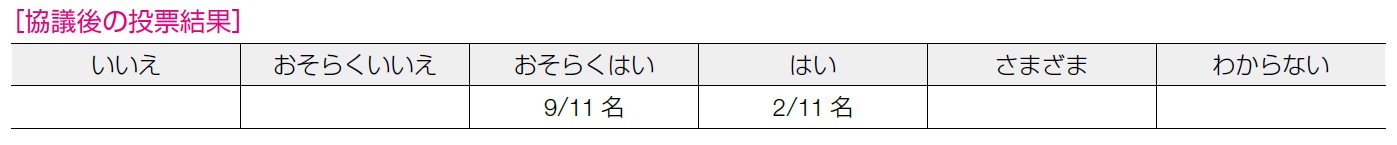
上記各検討項目の議論を踏まえたうえで,全員が「当該介入の条件付きの推奨」を選択した。TAMはすでに広く使われている薬剤であること,エビデンスは観察研究のみであるもののBRCA2 ではその効果が十分に期待できること,有害事象についても十分広く使用されている薬剤であることが指摘された。RRM 等,他のリスク低減手段を選択しない場合の代替手段として重要な治療であるとの認識がなされた。一方,今回参照した研究はBRCA1 とBRCA2 を分けておらず,今後の研究においてはそれぞれの遺伝子毎に検討する必要があるとの共通認識がなされた。

ASCO の乳癌リスク低減のための内分泌療法ガイドラインでは,乳癌発症高リスクの場合(家族歴や良性乳腺疾患罹患歴等)に化学予防が推奨されている。TAM 20 mg の5 年間内服が標準的な投与法として推奨されているものの,非浸潤癌を有する患者を対象とした臨床試験の結果から,それらの患者に対してはTAM 5 mg の3 年間内服がオプションとなり得ると記されている10)。なお,ASCO の遺伝性乳癌マネジメントガイドラインでは,内分泌療法を用いた化学予防については言及がない11)。
ESMO のHBOC ガイドラインでは乳癌既発症の場合,ホルモン受容体陰性であってもTAM の内服により対側乳癌のリスク低減が認められるものの,症例数が少ないこと等が指摘されている。そのため,CRRM を希望しない患者や耐術能がない患者に限定して,TAM の予防内服を検討すべきとされている12)。
NCCN のガイドラインでは,BRCA1/2 病的バリアント保持者に対するTAM 投与は他の乳癌ハイリスク因子と比較して十分な研究がされておらず,限定的な後ろ向き研究からはBRCA2 病的バリアント保持者でより高いリスク低減効果が期待し得るという記載にとどまっている13)。
日本乳癌学会の乳癌診療ガイドラインで同じCQ が取り上げられており,「BRCA1/2 病的バリアントを有する乳癌患者に対し,新規乳癌発症予防のために予防的内分泌療法を強く勧められるだけのデータは現時点ではない」と記載されている14)。
本CQ の問いのごとくBRCA1/2 病的バリアント保持者における化学予防の有用性は,TAM に着目した研究が多い中で,アロマターゼ阻害薬(aromatase inhibitor:AI)の有用性が示唆される結果が2022 年に新たに報告された。BRCA 遺伝学的検査が行われたエストロゲン受容体陽性乳癌患者935 例を対象とした観察研究において,BRCA1/2 とAI の内服に交互作用はなく(P =0.25),BRCA1/2 病的バリアント保持者にかかわらず,AI 内服により対側乳癌発症を低減し得ることが示された〔HR:0.46(95%CI:0.26-0.79)〕15)。今後,TAM 以外の予防的内分泌療法についても,エビデンスの蓄積が期待される。
本CQ のシステマティックレビューを行う過程で,本ガイドライン2021 年版と比較して新たなエビデンスは抽出されず,本CQ における臨床試験の難しさが明らかとなった。乳癌既発症者に対するTAM 投与の有効性を検証する臨床試験は実施されていない。一方で,未発症者に対する予防に関する臨床試験は国内外で実施されている。国外ではBRCA1 病的バリアント保持者を対象としてデノスマブを投与する試験16)が,わが国ではBRCA2 病的バリアント保持者を対象としてTAM 投与,MRIサーベイランス,リキッドバイオプシーを行う試験17)が実施されている。BRCA1 とBRCA2 では発症する乳癌のサブタイプが異なり,今後もBRCA1 とBRCA2 に分けた化学予防の開発が必要である
本CQ ではTAM の対側乳癌予防の意義について検討した。TAM は乳癌の術後治療としてサブタイプを問わず保険診療での処方が可能であるが,予防を目的として投与する場合は保険適用外となることに留意が必要である。
本CQ の結論についてはBRCA1 およびBRCA2 を区別せずにシステマティックレビューを実施した結果に留意が必要である。乳癌発症ハイリスク者に対するTAM による乳癌化学予防を評価した最大のランダム化比較試験であるNSABP-P1 試験で後ろ向きにBRCA1/2 病的バリアントを評価した研究では,BRCA2 でのTAM による乳癌発症予防効果が認められるものの,BRCA1 では認められていない。前述のように,BRCA1 とBRCA2 では発生する乳癌のサブタイプが異なっており,ホルモン受容体陽性の割合が大きく異なる(BRCA1 では70~80%がホルモン受容体陰性なのに対し,BRCA2 では70~80%がホルモン受容体陽性)。理論的にはホルモン療法はホルモン受容体陽性乳癌の発症を抑えると考えられるため,今後のガイドラインではBRCA1 とBRCA2 を分けた評価が必要である。現時点では結果が存在しないものの,BRCA1 病的バリアントに対するデノスマブを用いた予防研究や,わが国で実施されているBRCA2 病的バリアントに対するTAM を用いた予防研究があり,これらの結果によってそれぞれの遺伝子毎に今後は推奨が変わってくると考えられる
さらに,BRCA1/2 病的バリアントを保持する場合にはTAM の内服以外にも,MRI 等を用いたサーベイランスやRRM が選択肢となる。これらのオプションのうちどれを選択すべきかということについては検討されておらず,ガイドラインの適用の際には十分に患者と話し合うことが重要であり,また実際に患者がどのような選択肢を選ぶかについての観察研究も必要であろう。
外部評価団体より日本乳癌学会の乳癌診療ガイドラインとの違いに言及するよう指摘を受け,当該記述を追加した。
BRCA,Tamoxifen, chemoprevention,adverse event,cost,patient preference,patient satisfaction
文献検索式,エビデンス総体評価シート,システマティックレビューレポート,Evidence to Decisionフレームワークは,JOHBOC ホームページに掲載。
