Ⅱ-3 卵巣癌領域
BRCA1/2 病的バリアント保持者(BRCA1/2
関連卵巣癌)に対し,卵巣癌に対する初回薬物療法で用いられるプラチナ製剤併用レジメンを推奨する。
推奨のタイプ:当該介入の強い推奨
エビデンスの確実性:弱または中,合意率:92%(11/12 名)
推奨の解説:卵巣癌患者の初回薬物療法で用いるプラチナ系抗がん薬を含む化学療法はBRCA1/2 病的バリアント保持者において,非保持者と同等もしくはそれ以上の治療効果が得られており,初回薬物療法として治療することを推奨する。
卵巣癌の初回薬物療法では,プラチナ製剤併用レジメンが強く勧められるが,BRCA1/2 病的バリアントの有無によるレジメンの使い分けは行われていない。BRCA1/2 病的バリアントは,相同組換え修復欠損(HRD)と密接に関わり,プラチナ製剤への感受性が高いと考えられている。そのため,進行卵巣癌の初回治療において,BRCA1/2 病的バリアント保持者と非保持者で治療成績が異なる可能性が想定される。しかし,近年,血管新生阻害薬やPARP 阻害薬,免疫チェックポイント阻害薬など新しい薬剤の開発が進み,様々な併用療法の有用性が報告されている。初回薬物療法がさらに複雑化する前に,BRCA1/2 病的バリアント保持者と非保持者における治療成績を検証し,BRCA1/2 病的バリアント保持者へのプラチナ系抗がん薬を含む化学療法の治療的意義を明確にしておくことが重要である。なお,本CQ ではPARP 阻害薬を用いた報告は含めず,プラチナ製剤併用レジメンに焦点を当てて検討する。
BRCA1/2 病的バリアント保持者(BRCA1/2 関連卵巣癌)を対象として,初回薬物治療においてプラチナ系抗がん薬を含む化学療法で治療された群とプラチナ系抗がん薬を含まない化学療法で治療された群の比較ができなかった。そのため,本CQ では,プラチナ系抗がん薬を含む化学療法を行った場合のBRCA1/2 病的バリアント保持者と非保持者の2 群間で比較した際の「全生存期間(OS)」「無増悪生存期間」「有害事象」「費用対効果」「患者の意向」の5 項目を評価した。
本CQ に対する文献検索の結果,PubMed 393 編,Cochrane 95 編,医中誌 100 編が抽出され,計588 編がスクリーニング対象となった。2 名のシステマティックレビュー委員が独立して計2 回の文献スクリーニングを行い,抽出された9 編(メタ解析1 編,コホート7 編,症例対照研究1 編)を選択し,定性的なシステマティックレビューを行った。
抽出された9 編の中でOS に関する報告は,メタ解析1 編1)とコホート研究3 編2)~4)で示されている。いずれの解析においても,BRCA 病的バリアント保持者でのOS の有意な延長が示されている。ランダム化比較試験が0 編であり,エビデンスの確実性は弱と判断した。なお,BRCA1 病的バリアント保持者とBRCA2 病的バリアント保持者に分けて解析した場合,BRCA2 病的バリアント保持者においてOS がより良好な可能性が示されている4)
抽出された9 編の中で無増悪生存期間に関する報告は,メタ解析1 編1)とコホート研究4 編2)~5)で示されている。メタ解析1 編およびコホート研究3 編において,BRCA 病的バリアント保持者での無増悪生存期間の有意な延長が示されている。ただし,Tan らの症例対照研究ではBRCA 病的バリアント保持者22 名と遺伝的リスクの低い卵巣癌患者44 例との比較において無増悪生存期間に有意差を認めなかった(P=0.115)2)。ランダム化比較試験が0 編であり,エビデンスの確実性は弱と判断した。なお,BRCA1 病的バリアント保持者とBRCA2 病的バリアント保持者に分けて解析した場合,BRCA2病的バリアント保持者において無増悪生存期間がより良好な可能性が示されている。
抽出された9 編の中で有害事象に関する報告は,コホート研究3 編6)~8),症例対照研究1 編9)で示されている。Giannone らのコホート研究では,BRCA 病的バリアント保持者における過敏性反応(Hypersensitivity Reaction:HSR)のOR は2.14(95%CI:1.12-4.10),重篤なHSR のOR は2.19(95%CI:0.96-5.01)であった6)。また,Tomao らのコホート研究では,BRCA 病的バリアント保持者は非保持者に比べて有意に血液毒性が多く,G-CSF 投与のリスクOR は2.567(95%CI:1.136-5.798),化学療法遅延のリスクOR は3.860(95%CI:1.098-13.57)であった7)。Moon らのコホート研究では,BRCA 病的バリアント保持者のHSR OR は5.9(95%CI:1.1-31.7)であり,以前にHSR の既往がある場合にはOR 13.1(95%CI:2.6-65.4)と報告している8)。一方,Weitzner らの症例対照研究では,BRCA 病的バリアント保持者と非保持者との間に血液毒性に有意差を認めなかった9)。ランダム化比較試験が0 報であり,エビデンスの確実性は弱と判断した。
採用研究はなかった。
採用研究はなかった。
初回化学療法においてプラチナ製剤併用レジメンを用いた場合,BRCA 病的バリアント保持者は非保持者と比較しOS,無増悪生存期間ともに有意に延長することが,メタ解析も含め4 編で報告されている。
メタ解析では1996~2021 年の61 編(16,633 人の卵巣癌患者)のうち13 編でBRCA 病的バリアント保持者と非保持者のプラチナ系抗がん薬を含む化学療法に対する感受性について示されており,BRCA 病的バリアント保持者のほうが非保持者よりもプラチナ感受性があった。手術も含めた治療のアウトカムではあるが,BRCA 病的バリアント保持者でOS〔調整ハザード比:0.65(95%CI:0.59-0.73,P<0.001)〕,無増悪生存期間〔調整ハザード比:0.72(95%CI:0.63-0.82,P<0.001)〕と有意差を認めていた1)。
The Cancer Genome Atlas における316 例の高異型度漿液性癌の解析では,BRCA2 病的バリアント保持者が,非保持者に比べ,無増悪生存期間〔調整ハザード比:0.40(95%CI:0.22-0.74,P=0.004)〕,OS〔調整ハザード比:0.33(95%CI:0.16-0.69,P=0.003)〕とも有意に良好であった4)。一方,BRCA1 病的バリアント保持者については,非保持者に比べ,OS,無増悪生存期間ともに有意差がなかった。また,比較的小規模の後方視的解析では無増悪生存期間に有意差を認めないという報告もあった2)。
OS,無増悪生存期間いずれも,臨床病期Ⅲ,Ⅳ期のみの検討や,手術での残存腫瘍量に差がみられる検討等が混在しており,結果に影響している可能性が考えられた。また,乳癌罹患率に差がみられるものもあり,OS に影響している可能性がある。BRCA1 病的バリアント保持者とBRCA2 病的バリアント保持者で,個々に検討されているものとBRCA 病的バリアント保持者全体で検討されているものが混在しており,今後さらなる検討が必要である。
害のアウトカムとしてHSR に関する報告が4 編あり,そのうち3 編はBRCA 病的バリアント保持者においてHSR のリスクが上昇するという結果であった6)~8)。BRCA 病的バリアントは,HRD と密接に関わり,プラチナ製剤への感受性が高いため,BRCA 病的バリアント保持者は非保持者に比べ,プラチナ製剤併用レジメンでの治療回数が多くなる。そのため,BRCA 病的バリアント保持者では,プラチナ-DNA 複合体の産生量も増加し,IgE を介したアレルギー反応を引き起こしやすくなると考えられている。しかし,BRCA 病的バリアントの有無によってHSR の発症に有意差はないとする報告も1 編認めており9),さらなる検討が必要である。
本CQ の推奨決定会議参加対象委員12 名の内訳は,乳癌領域医師2 名,婦人科領域医師2 名,遺伝領域医師2 名,遺伝看護専門看護師1 名,認定遺伝カウンセラー2 名,患者・市民3 名であった。推奨決定会議の運営にあたっては,事前に資料を供覧し,参加対象委員全員がEvidence to Decision フレームワークを記入して意見を提示したうえで,当日の議論を行った。推奨決定会議には参加対象委員全員が参加した。
初回薬物療法としてプラチナ製剤併用レジメンは,標準的治療として確立しているが,BRCA 病的バリアントの有無で層別化されていないため,本CQ の優先度は高いと考えられた。また,現在様々な併用療法あるいは維持療法が検討されており,本CQ に対する直接的なエビデンスは今後増えない可能性がある。またがんゲノム医療の発展に伴い,臓器横断的なCQ の設定が必要との意見もあった。
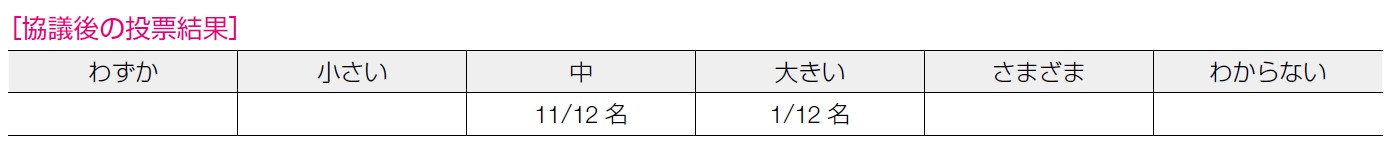
OS,無増悪生存期間の延長について期待できる結果が得られているが,手術完遂度等,化学療法以外の因子が関連する可能性があること,またBRCA1 とBRCA2 に分けて解析した場合の結果にばらつきを認めることが考慮され,望ましい効果について「中」が11 名であった。
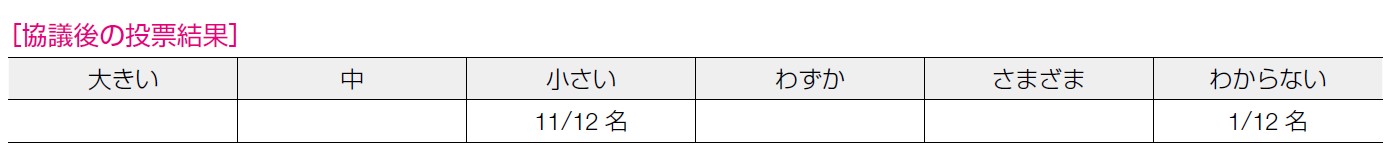
HSR については,プラチナ製剤併用レジメンでの治療回数の影響やBRCA 病的バリアントによる臨床薬理学的影響等を考慮する必要がある。また結果の非一貫性もあること,ランダム化比較試験もなく,報告数も限られていることから,介入の望ましくない効果について「小」が11 名であった。
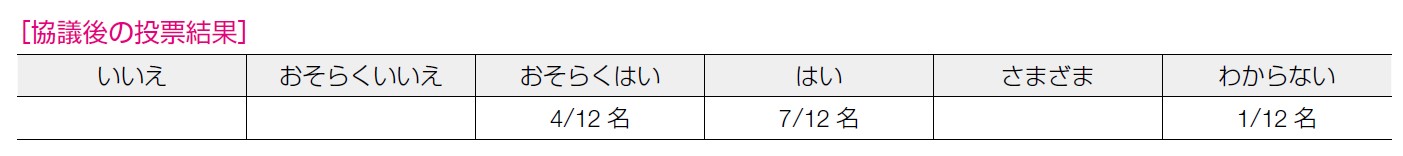
OS,無増悪生存期間,有害事象についてともにエビデンスの確実性は「弱」であり,エビデンスの確 実性として「弱」が7 名であった。OS,無増悪生存期間の延長というBRCA 病的バリアント保持者全 体への影響の強さも考慮され,5 名が「中」を選択した結果であった。

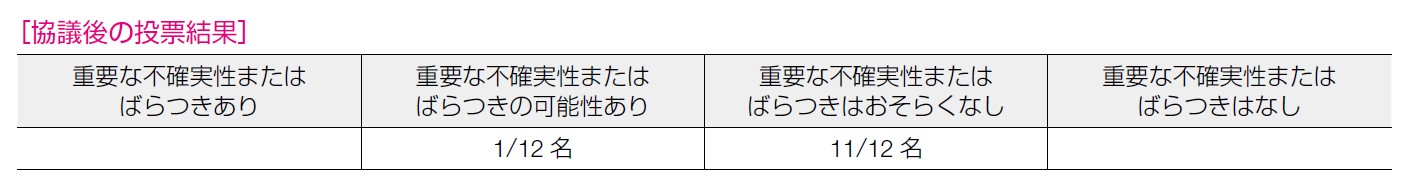
化学療法を必要とする卵巣癌患者において,今回設定されたアウトカムを重視する程度に重要なばらつきはなく,OS,無増悪生存期間延長という望ましい効果の確実性はその他の不確実性を十分に上回るものと考えられ,「重要な不確実性またはばらつきはおそらくなし」が11 名であった。
BRCA 病的バリアント保持者のほうが,非保持者と比較して無増悪生存期間,OS は良好であり,かつ有害事象として注目したHSR,血液毒性も対応が確立しており,生命を脅かす可能性が低いことから,プラチナ製剤併用レジメンがBRCA 病的バリアント保持者に対しても同様に推奨されることに優位性がある。

費用対効果に関する論文は抽出されなかった。

プラチナ製剤併用レジメンはすでに卵巣癌の初回薬物療法として確立しており,BRCA 病的バリアント保持者(BRCA 関連卵巣癌)に対しても同様に推奨されることが容認される。
プラチナ製剤併用レジメンは,卵巣癌初回薬物療法の標準的治療であり,保険診療として一般的に実施されており,実行可能である。

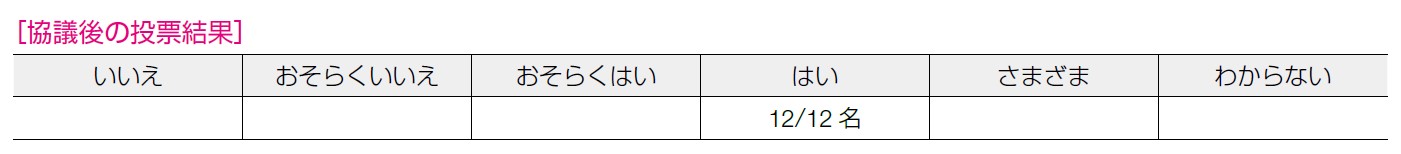
本CQ の優先度,望ましい効果と望ましくない効果とのバランス,エビデンスの確実性,価値観,容認性,実行可能性から判断され,本CQ の推奨タイプは「当該介入の強い推奨」が11 名であった。

NCCN ガイドライン10)では,メタ解析の結果として,BRCA 病的バリアント保持者は非保持者よりも5 年生存期間が有意に良好であるが10 年生存期間では両群間の差が少なくなると記載されている。また,BRCA2 病的バリアント保持者の予後が良好で,化学療法の奏効率が高いが,BRCA1 病的バリアント保持者では予後および化学療法奏効率との関係性が明らかでないと記載されている。
該当なし。
BRCA1/2 別の予後に関しては,引き続きモニタリングが必要である。また,BRCA 病的バリアント保持者とHSR のリスクとの関連性については,プラチナ製剤併用レジメンの治療回数に加え,BRCA 病的バリアントの臨床薬理学的影響等,遺伝学的要因も考慮しながらモニタリングしていく必要がある。
外部評価では内容に関する大きな指摘はなかった。
BRCA,ovarian cancer,chemotherapy,cost,patient preference
文献検索式,エビデンス総体評価シート,システマティックレビューレポート,Evidence to Decision フレームワークは,JOHBOC ホームページに掲載。
